题目内容
某实验小组的同学用碳酸钠粉末、颗粒状大理石、稀盐酸、浓盐酸、稀硫酸这几种药品,探究实验室制取CO2的反应原理.请你参与下列探究并回答问题.
[提出问题]上述几种酸和碳酸盐的反应是否适合在实验室制取CO2?
[问题说明](1)浓盐酸是否适合用于实验室制取CO2?请说明理由.
[方案设计]现有如下三个实验进行对比分析:
(2)请你完成实验报告中的有关内容的填写.
(3)根据探究结论,实验室制取二氧化碳的反应原理为______.
[拓展与迁移]
(4)由上述探究可知,在确定实验室制取气体的反应原理时,应该考虑哪些因素?(写出两点即可)
[提出问题]上述几种酸和碳酸盐的反应是否适合在实验室制取CO2?
[问题说明](1)浓盐酸是否适合用于实验室制取CO2?请说明理由.
[方案设计]现有如下三个实验进行对比分析:
(2)请你完成实验报告中的有关内容的填写.
| 实验 | 实验现象 | 得出的结论 |
| A | 剧烈反应,迅速放出大量气泡 | 反应速率过快,气体不便收集,不宜于实验室制取CO2 |
| B | 产生气泡,速率迅速减慢,反应几乎停止 | 无法持续产生CO2,不能用于实验室制取CO2 |
| C | ______ | ______ |
[拓展与迁移]
(4)由上述探究可知,在确定实验室制取气体的反应原理时,应该考虑哪些因素?(写出两点即可)

解;(1)因为浓盐酸易挥发出氯化氢气体,使制出的CO2不纯,因此浓盐酸不适合用于实验室制取CO2;(2)盐酸和大理石是实验室制取二氧化碳常用的药品,和A、B相比反应的现象是产生大量气泡,反应连续且持续时间较长;得出的结论是:反应速率适中,气体便于收集,因此可以用于实验室制取CO2;
(3)大理石和盐酸反应产生氯化钙、水和二氧化碳,反应的方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(4)由上述探究可知,在确定实验室制取气体的反应原理时,应该考虑的因素如:制得的气体较纯净,反应条件易满足,反应速率适中,不产生污染等.
故答案为:(3)CaCO3+2HCl═CaCl2+H2O+CO2↑;(4)制得的气体较纯净,反应条件易满足,反应速率适中,不产生污染等.
(3)大理石和盐酸反应产生氯化钙、水和二氧化碳,反应的方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(4)由上述探究可知,在确定实验室制取气体的反应原理时,应该考虑的因素如:制得的气体较纯净,反应条件易满足,反应速率适中,不产生污染等.
故答案为:(3)CaCO3+2HCl═CaCl2+H2O+CO2↑;(4)制得的气体较纯净,反应条件易满足,反应速率适中,不产生污染等.

练习册系列答案
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
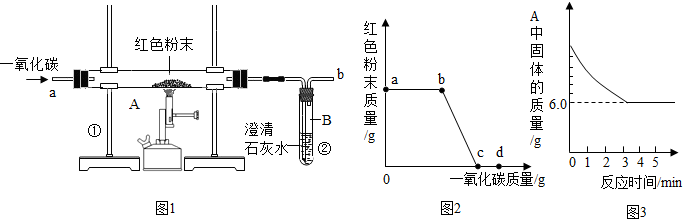
某科技小组的同学将16克氧化铜和过量的炭粉均匀混合,设计如图的实验装置进行探究.

请回答下列问题:
①仪器a和b的名称是:a ,b .
②装置a中的实验现象是 ;
装置c中发生反应的化学方程式为 .
③实验中最多能得到铜的质量为多少?(根据化学方程式列式计算)
答:
④同学们想通过测定消耗碳、氧元素的质量和生成二氧化碳的质量,以进一步分析氧化铜和炭粉反应产生的气体除CO2外是否还有其它产物.反应一段时间后停止加热,冷却到室温.反应前、后测得的数据如下:
分析数据发现,反应中消耗碳和氧元素的质量 (填“大于”或“小于”或“等于”)生成二氧化碳的质量.
⑤在保证装置不漏气、称量准确、操作规范,并且装置d中澄清石灰水不变浑浊的前提下,你认为导致上述④中结果可能的原因是:
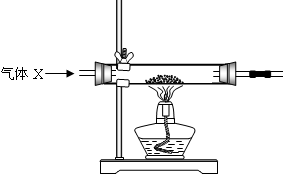
⑥有同学认为用下图装置代替上面的加热氧化铜和炭粉混合物的装置,加热前先通一会气体x,停止加热后再通一会该气体,这样可使实验测得的数据更能准确的说明问题.你认为在O2、N2和H2三种气体中,x应选择的气体是 .

请回答下列问题:
①仪器a和b的名称是:a
②装置a中的实验现象是
装置c中发生反应的化学方程式为
③实验中最多能得到铜的质量为多少?(根据化学方程式列式计算)
答:
④同学们想通过测定消耗碳、氧元素的质量和生成二氧化碳的质量,以进一步分析氧化铜和炭粉反应产生的气体除CO2外是否还有其它产物.反应一段时间后停止加热,冷却到室温.反应前、后测得的数据如下:
| 装置 | 反应前 | 反应后 |
| a | 试管的质量36.2g 氧化铜和炭粉混合物的质量为20.0g |
试管和固体物质的质量为54.8g |
| c | 反应后瓶内液体比反应前增重1.1g | |
⑤在保证装置不漏气、称量准确、操作规范,并且装置d中澄清石灰水不变浑浊的前提下,你认为导致上述④中结果可能的原因是:
⑥有同学认为用下图装置代替上面的加热氧化铜和炭粉混合物的装置,加热前先通一会气体x,停止加热后再通一会该气体,这样可使实验测得的数据更能准确的说明问题.你认为在O2、N2和H2三种气体中,x应选择的气体是

 24、同学们在探究碱溶液与酚酞溶液作用的实验时,发现了一个意外现象:向氢氧化钠溶液中滴入酚酞溶液(如图),溶液变成了红色,但是一会儿红色就消失了.为此某化学小组的同学进行了如下探究.
24、同学们在探究碱溶液与酚酞溶液作用的实验时,发现了一个意外现象:向氢氧化钠溶液中滴入酚酞溶液(如图),溶液变成了红色,但是一会儿红色就消失了.为此某化学小组的同学进行了如下探究. 维生素C是一种人体必需的维生素,查阅资料可知下列信息:
维生素C是一种人体必需的维生素,查阅资料可知下列信息: