题目内容
13.2013年,温州推行“河长制”:在每条“垃圾河、黑臭河”的河岸边竖起“河长公示牌”,明确河道责任人,促进河道环境的综合治理.最近有市民发现河边的某化工厂白天不排放污水,晚上偷排污水,就向“河长”进行举报.经“河长”和工作人员初步测量,认定污水中可能含有Fe3+、Ba2+、Na+、OH-、Cl-、SO42-等离子.为了进一步确认其污染物,他们进行实验分析检测.实验过程如下,请完成相应的问题.| 实 验 步 骤 | 实验现象 | 实验结论 |
| 1.取少量的污水,仔细观察. | 溶液呈无色、透明、不沉淀 | 没有Fe3+ |
| 2.①将一片pH试纸放在玻璃片上,用玻璃棒蘸取待测液滴到pH试纸上,将试纸呈现的颜色与标准比色卡比较 | pH试纸呈深蓝色 | 溶液的pH=13 |
| 3.取2毫升的污水,滴入稀硫酸溶液 | ②产生白色沉淀 | 污水中含有Ba2+ |
(2)根据以上实验结果,此工厂排放的污水中一定含有的污染物是氢氧化钡.
分析 (1)根据测定溶液pH具体操作步骤写出实验步骤即可,根据硫酸根离子遇到钡离子,生成硫酸钡白色沉淀考虑本题;(2)溶液呈无色、透明、不沉淀,说明没有Fe3+;pH试纸呈深蓝色,溶液的pH=13说明溶液显碱性,即含有OH-;滴入稀硫酸溶液,产生白色沉淀,说明含有Ba2+.根据溶液中离子共存的原理,含有钡离子,就一定不含硫酸根离子.再进行分析即可.
解答 解:(1)测定溶液pH具体操作步骤:将一片pH试纸放在玻璃片上,用玻璃棒蘸取待测液滴到pH试纸上,将试纸呈现的颜色与标准比色卡比较,就能测出pH值,硫酸根离子遇到钡离子,生成硫酸钡白色沉淀,所以现象是产生白色沉淀;
(2)溶液呈无色、透明、不沉淀,说明没有Fe3+;pH试纸呈深蓝色,溶液的pH=13说明溶液显碱性,即含有OH-;滴入稀硫酸溶液,产生白色沉淀,说明含有Ba2+.溶液中离子必须能够共存的原理,含有钡离子,就一定不含硫酸根离子.所以一定含有的污染物是氢氧化钡.
故答案为:(1)
| 实 验 步 骤 | 实验现象 | 实验结论 |
| 1.取少量的污水,仔细观察. | 溶液呈无色、透明、不沉淀 | 没有Fe3+ |
| 2.①将一片pH试纸放在玻璃片上,用玻璃棒蘸取待测液滴到pH试纸上,将试纸呈现的颜色与标准比色卡比较 | pH试纸呈深蓝色 | 溶液的pH=13 |
| 3.取2毫升的污水,滴入稀硫酸溶液 | ②产生白色沉淀 | 污水中含有Ba2+ |
点评 解答本题关键是知道铁离子溶液是黄色,熟悉离子共存问题,离子相互结合不能产生沉淀、气体或水.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目
3.下列关于原子核的叙述中正确的是( )
①原子核居于原子中心,带正电,所占体积很小;
②原子的质量主要集中在原子核上;
③构成原子核的质子、中子是不能再分的粒子;
④原子核的核电荷数等于核内中子数;
⑤原子核具有很高的密度;
⑥所有的原子都是由质子、中子和电子构成的.
①原子核居于原子中心,带正电,所占体积很小;
②原子的质量主要集中在原子核上;
③构成原子核的质子、中子是不能再分的粒子;
④原子核的核电荷数等于核内中子数;
⑤原子核具有很高的密度;
⑥所有的原子都是由质子、中子和电子构成的.
| A. | ①② | B. | ③④ | C. | ①②⑤ | D. | ③⑤⑥ |
8.将 2.1g的CO和H2组成的混合气体与足量氧气充分燃烧后,立即将全部燃烧产物通入足量的Na2O2固体(已知:2Na2O2+2CO2═2Na2CO3+O2、2Na2O2+2H2O═4NaOH+O2↑),充分反应后固体质量增加( )
| A. | 2.1g | B. | 2.4 g | C. | 3.6g | D. | 8.4g |
5.科学实验过程中,下列对意外事故的处理方法错误的是( )
| A. | 洒在桌面上的酒精燃烧起来,立即用湿抹布或沙子盖灭 | |
| B. | 浓硫酸不小心溅到皮肤上,先用干布擦拭,接着用大量的水冲洗,再涂上3%~5%的小苏打溶液 | |
| C. | 误服氯化钡溶液,立即喝大量鲜牛奶或鸡蛋清 | |
| D. | 碱液洒在衣服上,用水冲洗后,再涂上硫酸溶液 |
2.市场上出售的牙膏种类繁多,每种牙膏中都添加有细粉末状的摩擦剂,它能配合牙刷一起摩擦牙齿的表面,起到增强清洁牙齿的效果.下表给出了三种牙膏中的摩擦剂.
(1)可选作摩擦剂的物质必须难溶于水(填“易溶于水”或“难溶于水”).
(2)碳酸钙可用石灰石制备,小新设计了两种制备碳酸钙的实验方案.
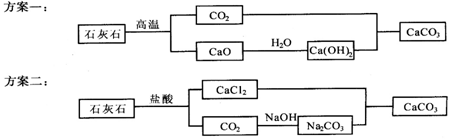
你认为哪一种实验方案更合理,并说明理由方案二,反应在通常情况下进行,生产效率高.
(3)小新为了测定B牙膏中碳酸钙的含量.称取B牙膏100克放入烧杯中,缓慢加入稀盐酸至不再有气泡产生(假设除碳酸钙外,牙膏中的其他物质不与盐酸反应),共用去稀盐酸200克.反应完毕后,称得烧杯内剩余物质的质量为278克.
①在测定中,反应生成的二氧化碳质量为22克.
②请计算牙膏中碳酸钙的质量分数.
| 牙膏 | A | B | C |
| 摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
(2)碳酸钙可用石灰石制备,小新设计了两种制备碳酸钙的实验方案.

你认为哪一种实验方案更合理,并说明理由方案二,反应在通常情况下进行,生产效率高.
(3)小新为了测定B牙膏中碳酸钙的含量.称取B牙膏100克放入烧杯中,缓慢加入稀盐酸至不再有气泡产生(假设除碳酸钙外,牙膏中的其他物质不与盐酸反应),共用去稀盐酸200克.反应完毕后,称得烧杯内剩余物质的质量为278克.
①在测定中,反应生成的二氧化碳质量为22克.
②请计算牙膏中碳酸钙的质量分数.
3.液化石油气作为燃料,已普遍进入城乡家庭,它是含有下列物质的混合物,在常压下,这些物质的沸点如下表所示:
在常温下使用至无气体放出时,钢瓶中常剩余的主要物质是( )
| 物质名称 | 乙烷 | 丙烷 | 丁烷 | 戊烷 | 己烷 |
| 沸点/℃ | -88.6 | -42.2 | -0.5 | 36.1 | 69.2 |
| A. | 乙烷、丙烷和丁烷 | B. | 乙烷和丙烷 | C. | 只有己烷 | D. | 戊烷和己烷 |