题目内容
将一块严重腐蚀而部分变成铜绿(化学式为Cu2(OH)2CO3)的铜块磨成粉末,在空气中充分灼烧成CuO,发现固体质量在灼烧成前后保持不变,则灼烧成前粉末中铜(单质)的质量分数为( )
| A、52.8% |
| B、50.0% |
| C、47.2% |
| D、46.3% |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:由在空气中充分灼烧而固体质量在灼烧前后保持不变的实验事实,可判断灼烧过程中铜与氧气反应生成氧化铜增加的质量和铜绿分解所放出水和二氧化碳而导致固体质量减少的质量相等;通过拟定增加与减少的质量利用两个反应的化学方程式分别计算出铜块中铜的质量与铜绿的质量,即可完成灼烧前粉末中铜的质量分数的计算.
解答:解:假设铜与氧气生成氧化铜增加的质量和铜绿分解放出二氧化碳、水而减少的质量为m,设粉末为铜的质量为x,铜绿的质量为y
2Cu+O2
2CuO 固体增加质量
128 32 160 160-128=32
x m
=
,
x=4m
Cu2(OH)2CO3
2CuO+H2O+CO2↑ 固体质量减少
222 160 222-160=62
y m
=
,
y=
m
灼烧前粉末中铜的质量分数=
×100%=52.8%
故选:A.
2Cu+O2
| ||
128 32 160 160-128=32
x m
| 128 |
| x |
| 3 |
| m |
x=4m
Cu2(OH)2CO3
| ||
222 160 222-160=62
y m
| 222 |
| y |
| 62 |
| m |
y=
| 111 |
| 31 |
灼烧前粉末中铜的质量分数=
| 4m | ||
4m+
|
故选:A.
点评:此类计算是运用化学中的基本思想质量守恒思想,通过归纳不同物质或不同变化过程中相同点和不同点有效地寻找出它们之间的内在联系以及融合点和嫁接点,体现创新思维能力.

练习册系列答案
相关题目
下列物质的用途与其依据的性质不相符合的是( )
| A、一氧化碳用于冶金工业--CO能够燃烧 |
| B、干冰用于人工降雨--干冰易升华同时吸收大量的热 |
| C、金刚石用于裁玻璃--金刚石硬度高 |
| D、石墨用于制铅笔芯--石墨质软有滑腻感 |
在CO2通过炽热的碳的反应中,下列说法正确的是( )
| A、CO被氧化,做还原剂 |
| B、C被氧化,做氧化剂 |
| C、CO2被还原,做氧化剂 |
| D、CO被还原,做还原剂 |
下列粒子在人体中起着重要的作用,其中属于阴离子的是( )
A、 |
B、 |
C、 |
D、 |
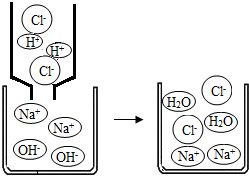 如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论错误的是( )
如图是氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图,由此得出的结论错误的是( )| A、反应结束时溶液的pH=7 |
| B、反应前后元素的种类没有变化 |
| C、该微观图还可说明所有物质都是由分子构成的 |
| D、酸与碱的反应属于复分解反应 |
已知一个碳原子的质量为a kg,如果另一种原子的质量为b kg,则该原子的相对原子质量为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
某学生为了验证铁、锌、铜三种金属的活动性顺序,设计了四种方案:①将Zn、Cu分别加入到FeSO4溶液中;②将Zn、Cu分别加入到ZnSO4溶液中;③将Fe分别加入到FeSO4、CuSO4溶液中;④将Fe分别加入到ZnSO4、CuSO4溶液中.其中可行的是( )
| A、①④ | B、①② | C、②③ | D、③④ |
化学式H2O所表示的意义中,错误的是( )
| A、表示水这种物质 |
| B、表示一个水分子由两个氢元素和一个氧元素组成 |
| C、表示水中含有氢元素和氧元素 |
| D、表示一个水分子由两个氢原子和一个氧原子构成 |
你认为下列实验方案中,可行的是( )
| A、按溶解、过滤、蒸发的操作顺序可以分离CaCl2、CaCO3的混合物 |
| B、向某未知溶液中加入AgNO3溶液,产生白色沉淀,证明溶液是盐酸 |
| C、用磷在密闭容器中燃烧,除去密闭容器内空气中的氮气 |
| D、将pH试纸润湿后,用玻璃棒蘸取食用白醋滴到试纸上,测定其pH |