题目内容
你认为下列实验方案中,可行的是( )
| A、按溶解、过滤、蒸发的操作顺序可以分离CaCl2、CaCO3的混合物 |
| B、向某未知溶液中加入AgNO3溶液,产生白色沉淀,证明溶液是盐酸 |
| C、用磷在密闭容器中燃烧,除去密闭容器内空气中的氮气 |
| D、将pH试纸润湿后,用玻璃棒蘸取食用白醋滴到试纸上,测定其pH |
考点:化学实验方案设计与评价,过滤的原理、方法及其应用,溶液的酸碱度测定,证明盐酸和可溶性盐酸盐,氧气的化学性质
专题:简单实验方案的设计与评价
分析:A、根据分离可溶性固体与液体可以使用过滤的方法进行解答;
B、根据银离子可以与氯离子和碳酸根离子结合生成白色沉淀进行解答;
C、根据磷不和氮气反应进行解答;
D、根据用PH试纸测定溶液的PH,试纸不能用水润湿进行解答.
B、根据银离子可以与氯离子和碳酸根离子结合生成白色沉淀进行解答;
C、根据磷不和氮气反应进行解答;
D、根据用PH试纸测定溶液的PH,试纸不能用水润湿进行解答.
解答:解:A、CaCl2易溶于水,而CaCO3不溶于水,可以使用溶解、过滤、蒸发的操作将其分离,故A正确;
B、银离子可以与氯离子和碳酸根离子结合生成白色沉淀,所以向某未知溶液中加入AgNO3溶液,产生白色沉淀,不能证明该溶液是盐酸,故B错误;
C、用磷在密闭容器中燃烧消耗氧气,生成的是固体五氧化二磷,但是磷不消耗氮气,所以不能用用磷除去密闭容器内空气中的氮气,故C错误;
D、用PH试纸测定食用白醋的PH,试纸不能用水润湿,否则造成溶液稀释,测定结果不准,故D错误.
故选A.
B、银离子可以与氯离子和碳酸根离子结合生成白色沉淀,所以向某未知溶液中加入AgNO3溶液,产生白色沉淀,不能证明该溶液是盐酸,故B错误;
C、用磷在密闭容器中燃烧消耗氧气,生成的是固体五氧化二磷,但是磷不消耗氮气,所以不能用用磷除去密闭容器内空气中的氮气,故C错误;
D、用PH试纸测定食用白醋的PH,试纸不能用水润湿,否则造成溶液稀释,测定结果不准,故D错误.
故选A.
点评:本题考查了实验方案的可行性,完成此题,可以依据物质的性质结合已有的知识进行.

练习册系列答案
相关题目
将一块严重腐蚀而部分变成铜绿(化学式为Cu2(OH)2CO3)的铜块磨成粉末,在空气中充分灼烧成CuO,发现固体质量在灼烧成前后保持不变,则灼烧成前粉末中铜(单质)的质量分数为( )
| A、52.8% |
| B、50.0% |
| C、47.2% |
| D、46.3% |
硒元素是人体必须的微量元素,具有抗癌作用,它的相对原子质量为79,其原子的核外电子数为34,则它的质子数为( )
| A、34 | B、45 | C、79 | D、113 |
某同学在量取10mL水时,视线仰视,则他量取的水的实际体积( )
| A、等于10mL |
| B、小于10mL |
| C、大于10mL |
| D、无法判断 |
对化学方程式2CO+O2
2CO2的读法或叙述正确的是( )
| ||
| A、一氧化碳加氧气点燃等于二氧化碳 |
| B、一氧化碳与氧气在点燃条件下生成二氧化碳 |
| C、反应中CO、O2、CO2的质量比为28:32:44 |
| D、2个一氧化碳分子加1个氧分子等于2个二氧化碳分子 |
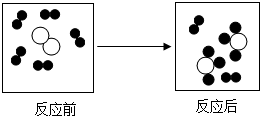
如图形象地表示某反应前后反应物与生成物的分子及其数目的变化,其中“ ”、“
”、“ ”、“
”、“ ”分别表示X、Y、Z三种不同的分子.该反应的化学方程式中X、Y、Z前的化学计量数之比为( )
”分别表示X、Y、Z三种不同的分子.该反应的化学方程式中X、Y、Z前的化学计量数之比为( )
 ”、“
”、“ ”、“
”、“ ”分别表示X、Y、Z三种不同的分子.该反应的化学方程式中X、Y、Z前的化学计量数之比为( )
”分别表示X、Y、Z三种不同的分子.该反应的化学方程式中X、Y、Z前的化学计量数之比为( )
| A、5﹕1﹕4 |
| B、10﹕2﹕12 |
| C、5﹕1﹕2:2 |
| D、3﹕1﹕2 |