题目内容
11.下表列出了除去物质中所含少量杂质的方法,其中错误的是( )| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | CO | CO2 | 通过足量氢氧化钠溶液,干燥 |
| B | NaCl | 泥沙 | 溶解、过滤、蒸发 |
| C | NaOH溶液 | Na2CO3 | 加入足量稀盐酸至不再产生气泡 |
| D | Cu(NO3)2溶液 | AgNO3 | 加入过量的铜粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、CO2能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,再干燥,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、氯化钠易溶于水,泥沙难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,故选项所采取的方法正确.
C、Na2CO3和NaOH溶液均能与足量稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
D、过量的铜粉能与AgNO3反应生成硝酸铜溶液和银,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:C.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
9.在实验室里鉴别下列物质的方法中,正确的是( )
| A. | 食盐和蔗糖:取样,分别尝味道 | |
| B. | 氧气和氮气:取样,分别闻气味 | |
| C. | 二氧化碳和氮气:取样,用燃着的木条检验 | |
| D. | 过氧化氢溶液和水:取样,分别加入少量二氧化锰 |
2.如图中的实验操作正确的是( )
| A. |  稀释浓硫酸 | B. |  除去CO中的CO2 | C. |  倾倒液体 | D. |  测定溶液的PH |
6.下列除去杂质(少量)的方法中,正确的是( )
| 选项 | 物质 | 杂质 | 除杂方法 |
| A | H2 | HCl | 通过饱和的Na2CO3溶液 |
| B | KNO3 | NaCl | 蒸发结晶 |
| C | NaCl | Na2CO3 | 加稍过量的稀盐酸,蒸发 |
| D | KCl | K2SO4 | 加稍过量Ba(NO3)2,蒸发 |
| A. | A | B. | B | C. | C | D. | D |
16.下列实验操作正确的是( )
| A. |  称量NaOH固体 | B. |  过滤 | ||
| C. |  稀释浓硫酸 | D. |  检查气密性 |
3.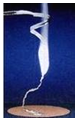 化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(如右图),同学们观察到镁条在空气中剧烈燃烧,发出耀眼的强光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体.
化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(如右图),同学们观察到镁条在空气中剧烈燃烧,发出耀眼的强光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体.
(1)请写出镁条燃烧的化学方程式2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;
(2)同学们通过称量发现:在石棉网上收集到产物的质量小于镁条的质量,有人认为这个反应不遵循质量守恒定律.你认为出现这样实验结果的原因可能是:生成的氧化镁小颗粒(白烟)扩散到空气中去了,使得生成物收集不全;
(3)小红按右下图装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体.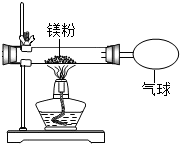
【提出问题】黄色固体是什么?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应产生黄色的氮化镁(Mg3N2)固体;③氮化镁可与水反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
【反思与交流】①氮化镁中氮元素的化合价是-3;
②空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是:氮气化学性质不如氧气活泼.
③同学们又联想到氯气在氧气中能够燃烧,于是对燃烧条件又有了新的认识:燃烧不一定需要氧气参加.
 化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(如右图),同学们观察到镁条在空气中剧烈燃烧,发出耀眼的强光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体.
化学兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验(如右图),同学们观察到镁条在空气中剧烈燃烧,发出耀眼的强光,产生的大量白烟弥漫到空气中,最后在石棉网上得到一些白色固体.(1)请写出镁条燃烧的化学方程式2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;
(2)同学们通过称量发现:在石棉网上收集到产物的质量小于镁条的质量,有人认为这个反应不遵循质量守恒定律.你认为出现这样实验结果的原因可能是:生成的氧化镁小颗粒(白烟)扩散到空气中去了,使得生成物收集不全;
(3)小红按右下图装置改进实验,验证了质量守恒定律,还发现产物中有少量黄色固体.

【提出问题】黄色固体是什么?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应产生黄色的氮化镁(Mg3N2)固体;③氮化镁可与水反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
| 实验操作 | 实验现象及结论 |
| 取少量黄色固体于试管中,加入适量的水,并将湿润的红色石蕊试纸放在试管口 | 试管中有气体产生,湿润的红色石蕊试纸变蓝.得出结论:黄色固体是Mg3N2 |
②空气中N2的含量远大于O2的含量,可是镁条在空气中燃烧产物MgO却远多于Mg3N2,合理的解释是:氮气化学性质不如氧气活泼.
③同学们又联想到氯气在氧气中能够燃烧,于是对燃烧条件又有了新的认识:燃烧不一定需要氧气参加.
1. 氢氧化镍是某种混合动力汽车电池的一种材料.镍原子结构示意图为Ni
氢氧化镍是某种混合动力汽车电池的一种材料.镍原子结构示意图为Ni
(1)镍原子最外层电子数是2;
(2)氢氧化镍的化学式为Ni(OH)2,从组成上看,它属于碱(选填“氧化物”、“酸”、“碱”、“盐”),预测该物质能与稀硫酸发生反应.
(3)按实验方案设计的路径,寻找两物质发生反应的证据.
查阅资料:①氢氧化镍:蓝绿色微溶于水的固体
②硫酸镍溶液呈绿色
③碳酸镍:浅绿色难溶于水的固体
 氢氧化镍是某种混合动力汽车电池的一种材料.镍原子结构示意图为Ni
氢氧化镍是某种混合动力汽车电池的一种材料.镍原子结构示意图为Ni(1)镍原子最外层电子数是2;
(2)氢氧化镍的化学式为Ni(OH)2,从组成上看,它属于碱(选填“氧化物”、“酸”、“碱”、“盐”),预测该物质能与稀硫酸发生反应.
(3)按实验方案设计的路径,寻找两物质发生反应的证据.
查阅资料:①氢氧化镍:蓝绿色微溶于水的固体
②硫酸镍溶液呈绿色
③碳酸镍:浅绿色难溶于水的固体
| 路径 | 步骤 | 现象 | 结论 |
| 反应物角度 | 取少量氢氧化镍(新制)悬浊液于试管中,向其中滴加过量稀硫酸,振荡 | ①悬浊液变澄清,溶液呈绿色(或蓝绿色沉淀消失,溶液呈绿色) | 氢氧化镍和稀硫酸反应的化学方程式 ④Ni(OH)2+H2SO4=NiSO4+2H2O |
| 生成物角度 | ②取上述澄清液少许于试管中,滴加过量NaOH溶液(或取上述澄清液少许于试管中,滴加过量Na2CO3溶液) | ③产生蓝绿色沉淀(或产生浅绿色沉淀) |
