题目内容
19.如图是一种医用药品瓶卜的标签,试根据标签如图下的内容回答有关问题.
(1)请叙述“咀嚼”后咽下的好处嚼碎后服用疗效快(答出一点即可)
( 2 )当胃酸(主要成分为盐酸)过多时,服用该药片后,在胃中可能发生的化学反应为(用化学方程式表示) ①MgCO3+2HCl=MgCl2+CO2↑+H2O,②Al(OH)3+3HCl=A1Cl3+3H2O.
( 3 )患有胃溃疡(胃勃膜溃烂)的病人胃酸过多时,不宜服用含碳酸盐的抗酸药,其原因是碳酸盐与盐酸作用生成二氧化碳气体,加重胃溃疡病情.
分析 (1)根据影响反应的因素来分析“咀嚼”后咽下的好处;
(2)根据信息可知物质的成分,利用物质的性质来分析与酸的反应;
(3)利用反应的生成物来分析胃溃疡(胃黏膜溃烂)的病人胃酸过多时,不宜服用含碳酸盐的抗酸药的原因.
解答 解:(1)因嚼碎后与反应物胃酸的接触面积增大,化学反应加快,则嚼碎后服用疗效快,故答案为:嚼碎后服用疗效快;
(2)由医用药品瓶上的标签可知,主要成分为碳酸镁和氢氧化铝,它们都能与盐酸反应,碳酸镁与盐酸反应生成氯化镁、水、二氧化碳,
氢氧化铝与盐酸反应生成氯化铝和水,故答案为:MgCO3+2HCl=MgCl2+CO2↑+H2O;Al(OH)3+3HCl=A1Cl3+3H2O;
(3)因碳酸盐与盐酸作用生成二氧化碳气体,能加重胃溃疡病情,故答案为:碳酸盐与盐酸作用生成二氧化碳气体,加重胃溃疡病情.
点评 本题考查学生利用医用药品瓶上的标签来抽取信息,并利用物质的性质及物质之间的化学反应来分析解答问题.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案
相关题目
9.以下说法中正确的是( )
| A. | 在H2S中,氢的化合价为+1价,硫的化合价为-2价 | |
| B. | 金属元素一定显正价,非金属元素一定显负价 | |
| C. | 一种元素只能表现一种化合价 | |
| D. | 氯气的化合价为零 |
10.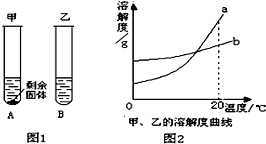 20℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质,使其充分溶解,可观察到如图所示的现象.
20℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质,使其充分溶解,可观察到如图所示的现象.
(1)20℃时,A(填“A”或“B”)试管中的溶液一定是饱和溶液;
(2)图2中表示甲物质的溶解度曲线的是b(填“a”或“b”),要使A试管中剩余的固体继续溶解可采用的方法是加水.
(3)20℃时,NaCl溶解于水的实验数据如下表.则下列叙述正确的是C.
A.②中所得溶液是饱和溶液
B.20℃时10g水最多能溶解4g NaCl
C.③④溶液的溶质质量分数相等
D.①所得溶液的溶质质量分数为20%
 20℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质,使其充分溶解,可观察到如图所示的现象.
20℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质,使其充分溶解,可观察到如图所示的现象.(1)20℃时,A(填“A”或“B”)试管中的溶液一定是饱和溶液;
(2)图2中表示甲物质的溶解度曲线的是b(填“a”或“b”),要使A试管中剩余的固体继续溶解可采用的方法是加水.
(3)20℃时,NaCl溶解于水的实验数据如下表.则下列叙述正确的是C.
| 实验序号 | 水的质量(g) | 加入NaCl的质量(g) | 溶液的质量(g) |
| ① | 10 | 2 | 12 |
| ② | 10 | 3 | 13 |
| ③ | 10 | 4 | 13.6 |
| ④ | 10 | 5 | 13.6 |
B.20℃时10g水最多能溶解4g NaCl
C.③④溶液的溶质质量分数相等
D.①所得溶液的溶质质量分数为20%
7.纯净物A可用作气体燃料,在一定条件下,将一定质量的A与160克B按如图所示充分反应,当B完全反应时,生成132克C和72克D.下列说法不正确的是( )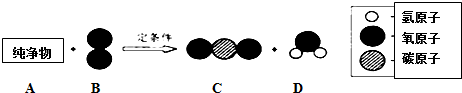

| A. | 生成C和D的分子个数比为3:4 | B. | 参加反应A的质量为44克 | ||
| C. | A中只含有碳元素和氢元素 | D. | 该反应为置换反应 |
14. 做菜用的一种嫩肉粉,其主要成分是碳酸氢钠(NaHCO3)可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软、鲜嫩.小明发现将拌了嫩肉粉的肉类放到锅中并加入食醋等调料烧煮时产生了大量气体.他对此颇感兴趣,决定对其进行探究.
做菜用的一种嫩肉粉,其主要成分是碳酸氢钠(NaHCO3)可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软、鲜嫩.小明发现将拌了嫩肉粉的肉类放到锅中并加入食醋等调料烧煮时产生了大量气体.他对此颇感兴趣,决定对其进行探究.
Ⅰ、小明对气体的成分进行了猜测:气体中除了醋酸气体之外,还可能含有水蒸气和CO2.
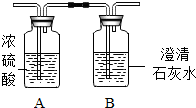
他设法收集气体样品并除去醋酸气体后,用如图实验装置进行探究.将气体依次通过A、B两试剂瓶后,发现A瓶质量增加,B瓶中有白色浑浊物产生.(已知浓硫酸具有吸水性)
实验结论:该气体中一定含有二氧化碳和水蒸气;
Ⅱ、小明对二氧化碳的来源做出了两种猜测:
猜测①二氧化碳可能是由碳酸氢钠受热分解产生的;
猜测②二氧化碳可能是由醋酸和碳酸氢钠反应生成的;
针对以上猜测,小明设计了以下实验:(请你填写如表)
Ⅲ、查阅资料:在百度网页中输入碳酸氢钠的化学性质,可以获知碳酸氢钠受热易分解,产物中有碳酸钠生成.再根据实验Ⅰ写出碳酸氢钠受热分解的化学方程式2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
Ⅳ、实验Ⅰ中有白色粉末剩余,请用两种化学方法来验证剩余粉末是碳酸钠(写出实验操作步骤、现象和结论);
方法一:取少量白色粉末,滴加稀盐酸,产生无色气体,并将气体通入澄清石灰水,石灰水变浑浊,则证明白色粉末为碳酸钠;
方法二:取少量白色粉末溶于水,加入适量氢氧化钙溶液,观察到溶液变浑浊,则证明白色粉末为碳酸钠.(其他合理答案均可).
 做菜用的一种嫩肉粉,其主要成分是碳酸氢钠(NaHCO3)可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软、鲜嫩.小明发现将拌了嫩肉粉的肉类放到锅中并加入食醋等调料烧煮时产生了大量气体.他对此颇感兴趣,决定对其进行探究.
做菜用的一种嫩肉粉,其主要成分是碳酸氢钠(NaHCO3)可破坏肉质纤维结构、促进肉类吸收水分,从而使肉质松软、鲜嫩.小明发现将拌了嫩肉粉的肉类放到锅中并加入食醋等调料烧煮时产生了大量气体.他对此颇感兴趣,决定对其进行探究.Ⅰ、小明对气体的成分进行了猜测:气体中除了醋酸气体之外,还可能含有水蒸气和CO2.
他设法收集气体样品并除去醋酸气体后,用如图实验装置进行探究.将气体依次通过A、B两试剂瓶后,发现A瓶质量增加,B瓶中有白色浑浊物产生.(已知浓硫酸具有吸水性)
实验结论:该气体中一定含有二氧化碳和水蒸气;
Ⅱ、小明对二氧化碳的来源做出了两种猜测:
猜测①二氧化碳可能是由碳酸氢钠受热分解产生的;
猜测②二氧化碳可能是由醋酸和碳酸氢钠反应生成的;
针对以上猜测,小明设计了以下实验:(请你填写如表)
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验1 | 取碳酸氢钠样品少许加入试管中,加热到不产生气体为止,并把产生的气体通入澄清石灰水 | 试管口有小水滴产生 澄清石灰水变浑浊 | 猜想①正确 |
| 实验2 | 取碳酸氢钠样品少许加入试管中,滴入适量醋酸,并把产生的气体通入澄清石灰水 | 产生气泡,样品逐渐消失,澄清石灰水变浑浊 | 猜想②正确 |
Ⅳ、实验Ⅰ中有白色粉末剩余,请用两种化学方法来验证剩余粉末是碳酸钠(写出实验操作步骤、现象和结论);
方法一:取少量白色粉末,滴加稀盐酸,产生无色气体,并将气体通入澄清石灰水,石灰水变浑浊,则证明白色粉末为碳酸钠;
方法二:取少量白色粉末溶于水,加入适量氢氧化钙溶液,观察到溶液变浑浊,则证明白色粉末为碳酸钠.(其他合理答案均可).
8.向Cu(NO3)2、AgNO3、Zn(NO3)2的混合溶液中加入一定质量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸有气泡产生,则滤出的固体物质中一定含有( )
| A. | Ag Cu Zn | B. | Ag Zn Fe | C. | Cu Zn Fe | D. | Ag Cu Fe |
 .
.