题目内容
9.下列物质中属于氧化物的是( )| A. | 空气 | B. | 氧气 | C. | 硫酸 | D. | 冰水混合物 |
分析 根据氧化物的概念可知,氧化物中只有两种元素且含有氧元素来分析解答.
解答 解:A、空气中含有氮气、氧气等多种物质,故属于混合物;
B、氧气是一种只有氧元素组成的物质,则属于单质,所以它不是氧化物;
C、硫酸是由H、O、S三种元素组成的物质,则不属于氧化物,
D、冰水混合物中只有一种物质就是水,水的化学式为H2O,它含有H和O两种元素且有氧元素的物质,则属于氧化物;
故选D
点评 本题考查氧化物的判断,学生应抓住氧化物概念的要点来判断,并要熟悉常见的物质的类别及相关概念.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
19.某化学兴趣小组的同学对碳酸钙高温加热一段时间剩余固体的成分进行探究.
【提出问题】剩余固体成分是什么?
【猜想与假设】
A.全部是碳酸钙 B.全部是氧化钙 C.①既有碳酸钙,也有氧化钙.
【设计并完成实验】
【实验结论】该化学兴趣小组同学得出的结论:
剩余固体成分应为【猜想与假设】中的④C(填“A”或“B”或“C”).
【交流与反思】实验操作(2)中产生的气体是⑤二氧化碳,该气体有何作用⑥:灭火(写一种即可).
【提出问题】剩余固体成分是什么?
【猜想与假设】
A.全部是碳酸钙 B.全部是氧化钙 C.①既有碳酸钙,也有氧化钙.
【设计并完成实验】
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体于试管中,加适量水振荡后静置,再滴几滴无色酚酞试液 | 溶液变红 | 说明固体成分中一定含有 ②氧化钙 |
| (2)再取少量固体于另一试管中滴加过量稀盐酸 | 有气泡生成 | 说明固体成分中一定含有③碳酸钙 |
剩余固体成分应为【猜想与假设】中的④C(填“A”或“B”或“C”).
【交流与反思】实验操作(2)中产生的气体是⑤二氧化碳,该气体有何作用⑥:灭火(写一种即可).
17.如表是几种家用清洁剂的功能和有效成分
据表回答下列问题:
(1)“洁厕灵”与马桶中污垢(主要成分为CaCO3)反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)在盛有少量二氧化锰的试管中,加入少量“活性彩漂”液体,观察到的现象是有大量气泡产生;
(3)“洁厕灵”与“漂白精”混合易产生一种气体X,反应的化学方程式为:NaClO+2HCl═NaCl+X↑+H2O,则X的化学式是Cl2,由此得出的一条生活经验是“洁厕灵”与“漂白精”不能混合使用.
| 清洁剂名称 | 洁厕灵 | 活性彩漂 | 漂白精 |
| 功能 | 清除马桶内的污垢 | 漂洗衣物,色彩更亮丽 | 快速漂除衣物污渍 |
| 有效成分 | HCl | H2O2 | NaClO(次氯酸钠) |
(1)“洁厕灵”与马桶中污垢(主要成分为CaCO3)反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)在盛有少量二氧化锰的试管中,加入少量“活性彩漂”液体,观察到的现象是有大量气泡产生;
(3)“洁厕灵”与“漂白精”混合易产生一种气体X,反应的化学方程式为:NaClO+2HCl═NaCl+X↑+H2O,则X的化学式是Cl2,由此得出的一条生活经验是“洁厕灵”与“漂白精”不能混合使用.
14.下列是四种粒子的结构示意图,一个说法中正确的是( )


| A. | 它们表示四种元素 | B. | ④属于阴离子 | ||
| C. | ③的元素在化合物中显+1价 | D. | ①和②的化学性质相似 |
1.下列为常见物质的pH,呈碱性的是( )
| A. |  牙膏pH=8.1 | B. |  食醋pH=2.2 | C. |  橙子pH=3.2 | D. |  苹果pH=4.0 |
18. 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?老师的帮助下,他们通过以下实验过程证明NaHCO3溶液与NaOH溶液发生了反应.
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?老师的帮助下,他们通过以下实验过程证明NaHCO3溶液与NaOH溶液发生了反应.
(1)【实验准备】
①查阅资料:NaHCO3+NaOH═Na2CO3+H2O
②用一定溶质的质量分数的NaHCO3、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考.
表中的现象Ⅰ为有气泡产生,现象Ⅱ对应反应的化学方程式为Ca(OH)2+Na2CO3=2NaOH+CaCO3↓.
(2)【实验过程】证明反应生成了Na2CO3
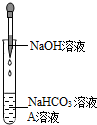
同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是CaCl2.
有同学提出这个实验不足以证明有Na2CO3生成,其理由是CaCl2 和NaOH反应生成Ca(OH)2,氢氧化钙是微溶物,在溶液中也产生沉淀.为了证明有Na2CO3生成,需要继续进行的操作是取少量反应后滤渣加入足量的稀盐酸,若产生无色气体证明有Na2CO3生成,反之则没有.
 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?老师的帮助下,他们通过以下实验过程证明NaHCO3溶液与NaOH溶液发生了反应.
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?老师的帮助下,他们通过以下实验过程证明NaHCO3溶液与NaOH溶液发生了反应.(1)【实验准备】
①查阅资料:NaHCO3+NaOH═Na2CO3+H2O
②用一定溶质的质量分数的NaHCO3、NaOH和Na2CO3三种溶液进行如下实验,为设计实验方案提供参考.
| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | 现象Ⅰ | 无明显变化 | 产生气泡 |
| 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
(2)【实验过程】证明反应生成了Na2CO3
同学们选用上表实验中的药品,设计了如图所示实验,先在NaHCO3溶液中加入A溶液,无明显现象,再滴加NaOH溶液,溶液变浑浊,则A溶液是CaCl2.
有同学提出这个实验不足以证明有Na2CO3生成,其理由是CaCl2 和NaOH反应生成Ca(OH)2,氢氧化钙是微溶物,在溶液中也产生沉淀.为了证明有Na2CO3生成,需要继续进行的操作是取少量反应后滤渣加入足量的稀盐酸,若产生无色气体证明有Na2CO3生成,反之则没有.
2.下列物品所使用的主要材料为有机合成材料的是( )
| A. |  纯棉毛巾 | B. |  陶瓷餐具 | C. |  塑料玩具 | D. |  玻璃钢桌椅 |
