题目内容
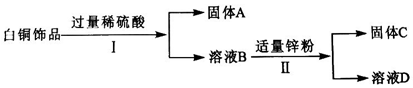
16.高纯碳酸钙广泛应用医药、生活和生产中,由工业副产品氯化钙(含有氯化亚铁和氯化镁)制取高纯碳酸钙的流程如图1:
【查阅资料】①氯化铵受热会分解.②室温下,氯化铵的溶解度随氯化钙的质量分数的变化关系如图2.
请回答下列问题:
(1)氯化钙、氨气、二氧化碳和水制取碳酸钙,同时生成NH4Cl的反应化学方程式为CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl.
(2)溶液A经蒸发浓缩、操作2、加入氯化钙、过滤等过程方可获得氯化铵固体,操作2的名称是冷却,加入适量氯化钙的目的是氯化铵的溶解度减小(填“增大”、“减小”或“不变”).
分析 根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,从给出的信息中找对应的信息.
解答 解:
(1)氯化钙、氨气、二氧化碳和水制取碳酸钙,同时生成NH4Cl,所以对应的反应化学方程式为 CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl.
(2)由于“氯化铵受热会分解溶液”所以制备氯化铵的过程温度不宜过高,所以采用蒸发浓缩,然后冷却,由于“室温下,氯化铵的溶解度随氯化钙的质量分数的变化关系,是氯化铵的溶解度随氯化钙的质量分数增大而减小”,所以加入氯化钙进一步降低氯化铵的溶解度使氯化铵最大量结晶析出.所以A经蒸发浓缩、操作2、加入氯化钙、过滤等过程方可获得氯化铵固体,操作2的名称是冷却(冷却结晶也可以),加入适量氯化钙的目的是氯化铵的溶解度减小(填“增大”、“减小”或“不变”).
故答案为:
(1)CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl.
(2)冷却(冷却结晶也可以); 减小.
点评 读图,从中获得解答题目所需的信息,所以在解答题目时先看解答的问题是什么,然后带着问题去读给出的图进而去寻找解答有用的信息,这样提高了信息扑捉的有效性.解答的问题实际上与复杂的转化图相比,其实很简单很基础,或者可以说转化图提供的是情境,考查基本知识.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案
相关题目
6.2016年12月《江西日报》报道:有权威排名机构绘制处全国“躲霾城市”20强,江西省新余、宜春等城市“榜上有名”.下列做法可能会导致雾霾产生的是( )
| A. | 使用清洁能源 | B. | 大量燃烧垃圾 | ||
| C. | 以步代车,绿色出行 | D. | 减少化石燃料的使用 |
7.将锌粉和铁粉的混合物加入盛有一定量硝酸银溶液的烧杯中,充分反应后过滤,将所得滤渣放入稀盐酸中,有气泡产生.下列说法错误的是( )
| A. | 滤液中最多含有两种溶质 | |
| B. | 滤液中一定含有Zn(NO3)2,可能含有Fe(NO3)2 | |
| C. | 滤渣里一定含有Fe和Ag,可能含有Zn | |
| D. | 若反应后所得滤液呈浅绿色,则滤渣中一定含有Fe和Ag,可能含有Zn |
11.今年3月22日是第27个世界水日,我国纪念“世界水日”“中国水周”活动的宣传主题为“落实绿色发展理念,全面推行河长制”,下列做法不符合以上主题的是( )
| A. | 加强河湖保护与管理 | B. | 开发水电清洁能源 | ||
| C. | 工业废水用来灌溉农田 | D. | 加强依法治水灌水 |
1.将无水硫酸亚铁(FeSO4)隔绝空气加强热,该反应的化学方程式为:2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO3+X,则X的化学式( )
| A. | SO2 | B. | O2 | C. | H2O | D. | S |
5.下列有关叙述中错误的是( )
| A. | 乙醇、沼气和氢气都是可再生能源 | |
| B. | 加速石油的开采,可以快速提高人类的生活质量 | |
| C. | “温室效应”加剧主要原因是大气中二氧化碳等气体含量升高引起的 | |
| D. | 为了防止水污染,农业上要合理使用化肥、农药 |
3.如图为元素周期表的一部分.下列叙述错误的是( )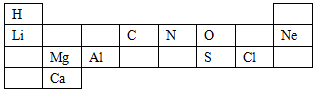

| A. | 钙的核电荷数是20 | |
| B. | 镁在化学反应中较易失去电子 | |
| C. | 每个周期结尾元素的化学性质比较稳定 | |
| D. | 硫离子的符号为是S2+ |