题目内容
1.为测定含小苏打的胃药的纯度(杂质不溶于水和酸,也不参与反应),取一定质量的胃药于烧杯中加热,一段时间后得到固体质量为13.8g,向其中加入100g7.3%的稀盐酸,充分反应后发现固体质量不在减少,过滤得一定质量的中性溶液和3.2g不溶物(滤渣),则该胃药中小苏打的纯度为( )| A. | 16% | B. | 84% | C. | 53% | D. | 无法计算 |
分析 碳酸氢钠受热可以生成碳酸钠和水和二氧化碳,根据:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,Na2CO3+2HCl=2NaCl+H2O+CO2↑,NaHCO3+HCl=NaCl+H2O+CO2↑一系列的反应可得碳酸氢钠与盐酸反应的关系式:NaHCO3 →HCl;根据盐酸的质量即可解得碳酸氢钠的质量,即可解答;
解答 解:设,碳酸氢钠样品中碳酸氢钠的质量为x,
根据:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,Na2CO3+2HCl=2NaCl+H2O+CO2↑,NaHCO3+HCl=NaCl+H2O+CO2↑一系列的反应可得碳酸氢钠与盐酸反应的关系式:
NaHCO3 →HCl
84 36.5
x 100g×7.3%
$\frac{84}{x}=\frac{36.5}{100g×7.3%}$,
x=16.8g
则原碳酸氢钠样品中碳酸氢钠的纯度:$\frac{16.8g}{16.8g+3.2g}×100%$=84%;
答案:B.
点评 在解答本题时需要注意到碳酸氢钠加热时时反应生成碳酸钠和水和二氧化碳,加热一段时间后得13.8g固体时,碳酸氢钠并没完全分解,需根据盐酸的质量来计算碳酸氢钠的质量.

练习册系列答案
相关题目
3.下列对于水的认识不正确的是( )
| A. | 构成:水是由氢原子和氧原子构成的 | |
| B. | 组成:水是由氢元素和氧元素组成的 | |
| C. | 变化:水结成冰发生的是物理变化 | |
| D. | 分类:是属于氧化物 |
4.下列实验装置或者实验方法正确的是( )
| A. |  制取收集CO2 | B. |  装入大理石 | C. |  干燥CO2气体 | D. |  CO2验满 |
1.下列图标中,表示“禁止烟火”的是( )
| A. |  | B. |  | C. |  | D. |  |
13.如图所示,下列实验操作正确的是( )
| A. | 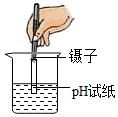 测溶液pH | B. |  称量氢氧化钠 | ||
| C. |  检查气密性 | D. |  稀释浓硫酸 |
 如图是探究甲烷中含有碳元素的实验;回答:
如图是探究甲烷中含有碳元素的实验;回答: 水是一切生命体的最基本组成成分,人类必须珍惜水.
水是一切生命体的最基本组成成分,人类必须珍惜水. A-H是初中化学中常见物质,已知A为金属氧化物,C为石灰石的主要成分,D为蓝色沉淀,G和H均为只含一种溶质的溶液,甲为镁粉和锌粉的混合物.“→”表示物质间存在相应的转化关系(部分生成物未标出),他们之间的关系如图所示,请回答下列问题:
A-H是初中化学中常见物质,已知A为金属氧化物,C为石灰石的主要成分,D为蓝色沉淀,G和H均为只含一种溶质的溶液,甲为镁粉和锌粉的混合物.“→”表示物质间存在相应的转化关系(部分生成物未标出),他们之间的关系如图所示,请回答下列问题: