题目内容
13.小科同学取一定质量分铝土矿(主要成分为Al2O3)于烧杯中,向其中加入40g20%的氢氧化钠溶液,恰好完全反应(Al2O3+2NaOH═2NaAlO2+H20),其中杂质不参与反应,反应结束后过滤得到滤渣的质量为2.5g,求该铝土矿中氧化铝的质量分数.分析 由题意,由氢氧化钠的质量、由反应的化学方程式、列式计算出参加反应的氧化铝的质量,进而计算出该铝土矿中氧化铝的质量分数.
解答 解:
设该铝土矿中氧化铝的质量为x,40g20%的氢氧化钠溶液中溶质质量=40g×20%=8g
Al2O3+2NaOH═2NaAlO2+H20
102 80
x 8g
$\frac{102}{x}=\frac{80}{8g}$
x=10.2g
该铝土矿中氧化铝的质量分数=$\frac{10.2g}{10.2g+2.5g}×$100%≈80.3%;
答案:该铝土矿中氧化铝的质量分数为80.3%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
1.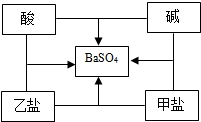 小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现图中所示的所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )
小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现图中所示的所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )
 小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现图中所示的所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )
小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现图中所示的所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )| A. | HCl NaOH BaCl2 Na2SO4 | B. | HCl Ba(OH)2 Na2SO4 BaCl2 | ||
| C. | H2SO4 Ba(OH)2 Na2SO4 BaCl2 | D. | H2SO4 NaOH BaCl2 Na2SO4 |
8.青少年缺锌会引起食欲不振,生长迟缓,发育不良,下列食物中富含锌元素的是( )
| A. |  西红柿 | B. |  青菜 | C. |  大海虾 | D. |  油酥烧饼 |
18.分离、提纯是化学实验的重要手段,下列方法中不能达到目的是( )
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | NaOH 溶液(Na2SO4) | 加入适量的Ba(OH)2溶液、过滤 |
| B | CaO(CaCO3) | 加水溶解、过滤 |
| C | O2(H2O) | 通入盛有浓硫酸的洗气瓶 |
| D | 铁粉(锌粉) | 加过量FeS04溶液充分反应后过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
5.如图表示水消毒时所发生反应的微观过程,下列有关说法正确的是( )


| A. | 反应前后分子和原子的数目都不变 | |
| B. | 该反应属于置换反应 | |
| C. | 反应后剩余了水,因此该反应不遵守质量守恒定律 | |
| D. | 生成物的水溶液呈中性 |
3.下列各组溶液,不用其他试剂就能鉴别出来的是( )
| A. | 稀H2SO4、KOH、CuSO4、MgCl2 | B. | Na2SO4、Ba(NO3)2、KNO3、NaCl | ||
| C. | BaCl2、稀HCl、Na2CO3、AgNO3 | D. | NaNO3、AgNO3、KCl、CaCl2 |
 在古代,黄金的真伪与成色(指金银制品中金银的纯度)的鉴定方法有很多.火烧法:真金用烈火烧不变色;假的灼烧后变黑褐色且失去光亮.
在古代,黄金的真伪与成色(指金银制品中金银的纯度)的鉴定方法有很多.火烧法:真金用烈火烧不变色;假的灼烧后变黑褐色且失去光亮.
