题目内容
1.通过一年的化学学习,相信你已经初步掌握了实验室制取气体的有关知识.请结合图示回答问题.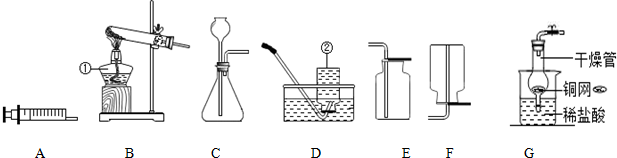
(1)写出图中标示的仪器名称:①酒精灯,②集气瓶
(2)实验室用高锰酸钾制取O2,应选用的发生和收集装置为BD或BE(选填字母),写出该反应的化学方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)注射器A在化学实验中有多种用途:
①将注射器A接在装置C右端导管处可用来检验装置的气密性;
②用注射器A替换装置C中的长颈漏斗(填仪器名称) 可组成优点更突出的发生装置.
(4)用G装置代替C装置制取CO2的优点是可以控制反应速率,用“铜网”不用“铁网”的原因是铁可以与稀盐酸反应,生成氢气,影响二氧化碳的纯度.
分析 (1)熟悉常见仪器,了解名称;
(2)根据实验室用KMnO4制取O2,是固体的加热反应选择实验的发生装置;根据氧气的密度和溶解性选择收集装置;
(3)根据将注射器A连接到装置C的导管口处,缓慢拉动注射器A的活塞,观察现象,可以检查气密性解答;
(4)根据装置特点分析解答;根据化学性质活泼与稀盐酸反应生成氢气解答.
解答 解:(1)图中①是酒精灯,②是集气瓶.
故答案为:①酒精灯;②集气瓶.
(2)实验室用KMnO4制取O2,是固体的加热反应,所以选择发生装置B进行实验;氧气的密度大于空气的密度,并且不易溶于水,所以可以用排水法和向上排空气法收集;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)①将注射器A接在装置C右端导管处可用来检查装置的气密性;
②注射器与长颈漏斗比较,注射器上有可以控制的活塞,可以根据实验时的需要控制添加药品的速度,故可控制反应速率,不用时可随时停止,又可节约药品用注射器A替换装置C中的长颈漏斗可组成优点更突出的发生装置.
(4)用G装置代替C装置制取CO2的优点是可以控制反应速率;铁化学性质活泼与稀盐酸反应生成氢气,使生成的二氧化碳不纯,铜化学性质不活泼不与稀盐酸反应.
故答案为:
(1)酒精灯;集气瓶;
(2)BD或BE;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)①检查装置的气密性;③长颈漏斗.
(4)可以控制反应速率(合理均可);铁可以与稀盐酸反应,生成氢气,影响二氧化碳的纯度.
点评 根据反应物的状态和反应条件选择发生装置,据气体的密度和溶解性选择收集装置,并掌握检查气密性的方法,能对装置进行正确评价是解答此题的关键.

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案| A. | 氧气具有助燃性,可用于焊接和切割金属 | |
| B. | 氮气是空气中含量最高的气体,可以用来保护粮食等 | |
| C. | 空气中过多二氧化碳的排放,是造成酸雨的主要原因 | |
| D. | 少量有害物质进入空气中,依靠大自然的自我洁净能力,空气仍能保持洁净 |
| A. |  加热液体 | B. |  蒸发食盐水 | C. |  测溶液的pH | D. |  稀释浓硫酸 |
| A. | 氢氧化钠固体露置在空气中,表面变潮湿-氧化 | |
| B. | 用洗洁精洗去油污-溶解 | |
| C. | 冷却热的硝酸钾饱和溶液,出现晶体-蒸发 | |
| D. | 打开装有浓盐酸的试剂瓶瓶塞,瓶口出现白雾-挥发 |
| A. | 血红蛋白中含有铁元素,缺铁会引起人体贫血 | |
| B. | 回收废弃的塑料可以减少“白色污染” | |
| C. | 肥皂水可以区分硬水和软水 | |
| D. | 汽油着火可用水扑灭 |
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | Na2CO3溶液呈碱性 | Na2CO3属于碱 |
| B | 分子之间有间隔 | 浓氨水和浓盐酸接近时“空中生烟” |
| C | 金属Al是热的良导体 | 金属Al可以用来制作生活炊具 |
| D | 二氧化碳不支持燃烧 | 二氧化碳能使澄清石灰水变浑浊 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 氧气 | B. | 水 | C. | 氧化钾 | D. | 氢氧化钠 |
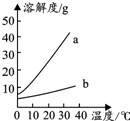 如图是Na2CO3、NaHCO3的溶解度表及溶解度曲线.
如图是Na2CO3、NaHCO3的溶解度表及溶解度曲线. | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3的溶解度(g/100g水) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3的溶解度(g/100g水) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
(2)10℃时,在100g水中加入20g碳酸钠固体,所形成的溶液中碳酸钠的质量分数为11%(精确到1%)
(3)实验室中要除去Na2CO3固体中的少量NaHCO3的物理方法的操作步骤是:溶解,结晶降温(填“降温”或“蒸发”),过滤.
(4)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O═2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是通入足量的二氧化碳.

