题目内容
11.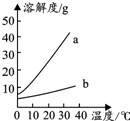 如图是Na2CO3、NaHCO3的溶解度表及溶解度曲线.
如图是Na2CO3、NaHCO3的溶解度表及溶解度曲线. | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | |
| Na2CO3的溶解度(g/100g水) | 7.1 | 12.5 | 21.5 | 39.7 | 49.0 |
| NaHCO3的溶解度(g/100g水) | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 |
(2)10℃时,在100g水中加入20g碳酸钠固体,所形成的溶液中碳酸钠的质量分数为11%(精确到1%)
(3)实验室中要除去Na2CO3固体中的少量NaHCO3的物理方法的操作步骤是:溶解,结晶降温(填“降温”或“蒸发”),过滤.
(4)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O═2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是通入足量的二氧化碳.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度表中的数据可知,Na2CO3溶解度曲线为a;
(2)10℃时,碳酸钠的溶解度是12.5g,所以在100g水中加入20g碳酸钠固体,所形成的溶液中碳酸钠的质量分数为$\frac{12.5g}{100g+12.5g}$×100%=11%;
(3)碳酸钠的溶解度受温度变化影响较大,所以实验室中要除去Na2CO3固体中的少量NaHCO3的物理方法的操作步骤是:溶解,降温结晶,过滤;
(4)已知Na2CO3转化为NaHCO3的反应为Na2CO3+CO2+H2O═2NaHCO3,根据以上信息,要除去NaHCO3饱和溶液中的少量Na2CO3,应采用的化学方法是:通入足量的二氧化碳.
故答案为:(1)a;
(2)11%;
(3)降温;
(4)通入足量的二氧化碳.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
2.下列除去杂质(括号内)的方法正确的是( )
| A. | CO2(CO):通过灼热的氧化铜 | B. | KOH溶液(K2CO3):加适量稀盐酸 | ||
| C. | Ba(NO3)2(BaCl2):溶于水过滤 | D. | 锌粉(硫酸锌粉末):加入足量稀硫酸 |
19.下列物质露置在空气中 质量减小的是( )
| A. | 氢氧化钠 | B. | 浓硫酸 | C. | 浓盐酸 | D. | 氯化钠 |
16.下列混合物,能按“溶解-过滤-蒸发”的步骤加以分离的是( )
| A. | 石灰石和大理石 | B. | 纯碱和蔗糖 | C. | 水和酒精 | D. | 食盐和细砂 |
3.下列作法不符合环保理念的是( )
| A. | 为预防传染病不回收塑料制品 | B. | 禁止在公共场所吸烟 | ||
| C. | 秸秆回收利用,不露天焚烧 | D. | 提倡使用风力发电 |
20.生产、生活中的很多现象与变化有关,属于化学变化的是( )
| A. | 冰雪融化 | B. | 水的净化 | C. | 燃料燃烧 | D. | 风力发电 |