题目内容
2.现有一固体混合物A,已知其中可能含有CuCaO、NaCO3、(NH4)2SO2、BaCl2四种物质中的两种或多种.按如图进行实验,出现的现象如图所示(设过程中所有可能发生的反应均恰好完全反应).
试根据实验过程和发生的现象填写以下空白:
(1)产生的气体B是(写化学式)CO2;
(2)混合物A中,肯定存在的物质是(写化学式)Na2CO3、Cu、BaCl2;一定存在3种物质;
(3)溶液C 中,一定存在的酸根离子是(写符号)S${{O}_{4}}^{2-}$;E的化学式为Cu;
(4)写出实验过程③中一定发生反应的化学方程式为CuSO4+Fe=FeSO4+Cu.
(5)通过上述过程,有一种物质尚无法确定是否存在于混合物A中,这种物质应该如何检验?请写出你的步骤、现象、和结论取样品,加入熟石灰研磨,有刺激性气味的气体产生,说明混合物中一定含有硫酸铵.
分析 根据铜和氧气、硫酸加热会生成硫酸铜和水,氧化钙和水反应生成氢氧化钙,氢氧化钙和铵根离子反应会生成氨气,硫酸根离子和钡离子反应会生成硫酸钡沉淀等知识进行分析.
解答 解:铜和氧气、硫酸加热会生成硫酸铜和水,氧化钙和水反应生成氢氧化钙,氢氧化钙和铵根离子反应会生成氨气,硫酸根离子和钡离子反应会生成硫酸钡沉淀.
滤液C和铁反应会生成红色固体,所以C中含有硫酸铜,固体混合物中含有铜,白色沉淀D加硝酸不溶解,所以D是硫酸钡沉淀,混合物中一定氯化钡,气体B能使紫色石蕊试纸变红色,所以B是二氧化碳,所以混合物中一定含有碳酸钠,一定不含氧化钙,硫酸会引入硫酸根离子,混合物中可能含有硫酸铵,所以
(1)产生的气体B是:CO2;
(2)混合物A中,肯定存在的物质是:Na2CO3、Cu、BaCl2;一定存在3种物质;
(3)溶液C 中,一定存在的酸根离子是:S${{O}_{4}}^{2-}$;E的化学式为Cu;
(4)实验过程③中一定发生的反应是铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:CuSO4+Fe=FeSO4+Cu;
(5)通过上述过程,有一种物质尚无法确定是否存在于混合物A中,这种物质检验的方法是:取样品,加入熟石灰研磨,有刺激性气味的气体产生,说明混合物中一定含有硫酸铵.
故答案为:(1)CO2;
(2)Na2CO3、Cu、BaCl2;3;
(3)S${{O}_{4}}^{2-}$;Cu;
(4)CuSO4+Fe=FeSO4+Cu;
(5)取样品,加入熟石灰研磨,有刺激性气味的气体产生,说明混合物中一定含有硫酸铵.
点评 在解此类题时,首先分析所给混合物中各物质的性质,然后根据题中所给的实验现象进行判断,最后确定混合物的组成成分.

练习册系列答案
相关题目
10.地壳中含量最多的元素是( )
| A. | 氧元素 | B. | 氮元素 | C. | 铝元素 | D. | 钠元素 |
17.将5.6g某金属片放入足量的稀盐酸中,充分反应后生成0.2g氢气,则该金属可能是( )
| A. | 铝-铁合金 | B. | 镁-锌合金 | C. | 锌-铁合金 | D. | 铁-铜合金 |
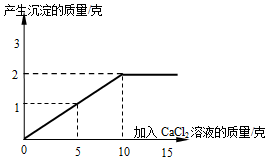 实验室有一瓶敞口存放的氢氧化钠,小明在做实验时发现已部分变质.他称取变质的氢氧化钠样品15克放入烧杯,加适量蒸馏水配制成溶液,再向其中滴加CaCl2溶液(反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl).反应时CaCl2溶液与沉淀的质量关系如图所示.请解决以下问题:
实验室有一瓶敞口存放的氢氧化钠,小明在做实验时发现已部分变质.他称取变质的氢氧化钠样品15克放入烧杯,加适量蒸馏水配制成溶液,再向其中滴加CaCl2溶液(反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl).反应时CaCl2溶液与沉淀的质量关系如图所示.请解决以下问题: