题目内容
3.氧烛是一种用于缺氧环境中自救的化学氧源,广泛用于航空、航海等领域,其主要成分为NaClO3,还含有适量的催化剂、成型剂等.氧烛通过撞击火帽引发反应后,能持续放出高纯氧气,主要反应原理为2NaClO3═2NaCl+3O2↑.一根氧烛大约可以供100个人呼吸1小时.下列说法不正确的是( )| A. | 氧烛是一种纯净物 | B. | NaClO3中Cl为+5价 | ||
| C. | 氧烛制取氧气的反应为分解反应 | D. | 在运输氧烛时,应避免其受到撞击 |
分析 A、根据题意,氧烛的主要成分为NaClO3,还含有适量的催化剂、成型剂等,进行分析判断.
B、根据在化合物中正负化合价代数和为零,进行分析判断.
C、根据氧烛制取氧气的反应为2NaClO3═2NaCl+3O2↑,进行分析判断.
D、根据题意,氧烛通过撞击火帽引发反应后,能持续放出高纯氧气,进行分析判断.
解答 解:A、氧烛的主要成分为NaClO3,还含有适量的催化剂、成型剂等,属于混合物,故选项说法错误.
B、钠元素显+1价,氧元素显-2价,设氯元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)+x+(-2)×3=0,则x=+5价,故选项说法正确.
C、氧烛制取氧气的反应为2NaClO3═2NaCl+3O2↑,该反应符合“一变多”的特征,属于分解反应,故选项说法正确.
D、氧烛通过撞击火帽引发反应后,能持续放出高纯氧气,在运输氧烛时,应避免其受到撞击,故选项说法正确.
故选:A.
点评 本题难度不大,理解氧烛的主要成分、化学性质等,掌握混合物与纯净物的判别方法、化合物中正负化合价代数和为零等是正确解答本题的关键.

练习册系列答案
相关题目
5.下列各组物质按照单质、混合物、氧化物的顺序分类正确的是( )
| A. | 铁、食盐水、过氧化氢 | B. | 氨气、空气、胆矾 | ||
| C. | 石墨、大理石、海水 | D. | 冰、稀盐酸、五氧化二磷 |
2.我国政府高度重视实施可持续发展战略,明确提出建立节约型社会.节约能源,应从我们身边做起,下列做法正确的是( )
| A. | 为了QQ能够升级,长期把QQ挂在线上 | |
| B. | 天气太热,中午放学后,开着电风扇给教室降温 | |
| C. | 夏天洗澡擦肥皂时,关上喷头 | |
| D. | 双面草稿纸只用一面就丢弃 |
9.聚乳酸是一种新型可生物降解的高分子材料,可用于制造可降解塑料.聚乳酸由乳酸(CH3-CHOH-COOH)在催化剂作用下聚合而成.下列说法不正确的是( )
| A. | 乳酸属于有机化合物 | B. | 使用聚乳酸不会造成白色污染 | ||
| C. | 乳酸中氧元素质量分数最大 | D. | 乳酸由碳原子、氢原子、氧原子成 |
15.固体水,也叫干水,它内含98%以上的水分,是一种集微生物和化学技术为一体的生态环保产品.在常温下,不流动、不蒸发、摄氏0℃不结冰,在100℃也不融化.它的外观看起来更像是有弹性的胶状体.下列关于固体水的说法中正确的是( )
| A. | 固体水属于氧化物 | B. | 固体水和普通水的化学性质相同 | ||
| C. | 固体水中水分子不运动 | D. | 固体水在自然界会对环境造成污染 |
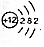 和
和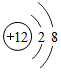 ,它们表示的是同种元素;
,它们表示的是同种元素;