题目内容
12.诺贝尔奖获得者屠呦呦发现的青蒿素,化学式为C15H22O5,请计算:(1)青蒿素中碳、氧元素的质量比为9:4.
(2)28.2g青蒿素中含氢元素的质量为多少g.
分析 (1)化合物中各元素质量比为各元素的相对原子质量之和的比;
(2)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)青蒿素中碳、氧三种元素的质量比为(12×15):(16×5)=9:4;故填:9:4;
(2)C15H22O5的相对分子质量为:(12×15)+(1×22)+(16×5)=282
28.2g青蒿素中含氢元素的质量为28.2g×$\frac{1×22}{282}$×100%=2.2g.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.下列物质中,氮元素的化合价为+4价的是( )
| A. | N2 | B. | NH3 | C. | NO2 | D. | KNO3 |
3.氧烛是一种用于缺氧环境中自救的化学氧源,广泛用于航空、航海等领域,其主要成分为NaClO3,还含有适量的催化剂、成型剂等.氧烛通过撞击火帽引发反应后,能持续放出高纯氧气,主要反应原理为2NaClO3═2NaCl+3O2↑.一根氧烛大约可以供100个人呼吸1小时.下列说法不正确的是( )
| A. | 氧烛是一种纯净物 | B. | NaClO3中Cl为+5价 | ||
| C. | 氧烛制取氧气的反应为分解反应 | D. | 在运输氧烛时,应避免其受到撞击 |
20.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
| A. | 在空气中点燃纯净的氢气,火焰为淡蓝色,说明氢气能支持燃烧 | |
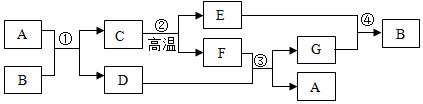
| B. | 高温下,将一氧化碳通过氧化铁粉末,黑色粉末变为红色,说明一氧化碳具有还原性 | |
| C. | 将铁丝和铜丝分别放入稀盐酸中,铁丝表面有气泡产生,铜丝表面无变化,说明铁的金属活动性比铜强 | |
| D. | 将二氧化碳通入紫色石蕊溶液中,紫色石蕊溶液变成红色,说明二氧化碳显酸性 |
1.为补充维生素C,医生可能会建议该同学饮食中适量增加( )
| A. | 面食 | B. | 植物油 | C. | 瘦肉 | D. | 蔬菜、水果 |
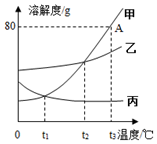
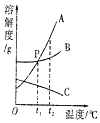 如图是A、B、C三种固体物质的溶解度曲线,请回答:
如图是A、B、C三种固体物质的溶解度曲线,请回答: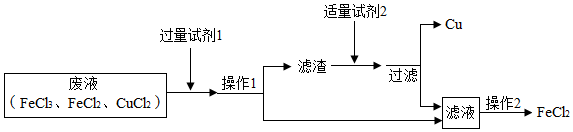
 人类的生活离不开能源、资源与营养物质.请回答下列问题:
人类的生活离不开能源、资源与营养物质.请回答下列问题: