题目内容
(1)科学施肥是实现农业增产的重要手段.硝酸铵(NH4NO3)是一种常用的氮肥,其中氮、氢、氧三种元素的质量比为 .若要配制200g溶质质量分数为5%的硝酸铵溶液,需要硝酸铵的质量为 g,需要水的质量为 g.
(2)实验室有一瓶硫酸溶液,老师请小红同学设计方案测定该废液中硫酸的质量分数.小红同学先取一洁净小烧杯,称其质量为18.2g,然后往其中倒入少量硫酸废液后称量,总质量为33.2g,之后,将一枚质量为10.8g的铁钉(已用砂纸打磨去铁锈)放入该小烧杯中反应,待铁钉表面不再有气泡产生后,再次称量,总质量为43.9g.请回答下列问题:
①写出上述反应的化学方程式 .
②反应中产生的气体的质量是 g.
③该废液中硫酸的质量分数为 .
④若铁钉的铁锈未除净,对计算结果的影响是 (选“偏大”、“偏小”、“无影响”),原因是 .
(2)实验室有一瓶硫酸溶液,老师请小红同学设计方案测定该废液中硫酸的质量分数.小红同学先取一洁净小烧杯,称其质量为18.2g,然后往其中倒入少量硫酸废液后称量,总质量为33.2g,之后,将一枚质量为10.8g的铁钉(已用砂纸打磨去铁锈)放入该小烧杯中反应,待铁钉表面不再有气泡产生后,再次称量,总质量为43.9g.请回答下列问题:
①写出上述反应的化学方程式
②反应中产生的气体的质量是
③该废液中硫酸的质量分数为
④若铁钉的铁锈未除净,对计算结果的影响是
考点:元素质量比的计算,有关溶质质量分数的简单计算,根据化学反应方程式的计算
专题:化学式的计算,溶液的组成及溶质质量分数的计算,有关化学方程式的计算
分析:(1)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得蒸馏水的质量.
(2)①根据质量守恒定律正确书写化学方程式,
②铁和稀硫酸反应生成硫酸亚铁和氢气,根据质量差可以求生成氢气的质量;
③根据氢气的质量求出硫酸中溶质的质量,从而求出废液中硫酸的质量分数即可;
④根据铁钉的铁锈未除净,则铁锈消耗一部分硫酸进行解答.
利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得蒸馏水的质量.
(2)①根据质量守恒定律正确书写化学方程式,
②铁和稀硫酸反应生成硫酸亚铁和氢气,根据质量差可以求生成氢气的质量;
③根据氢气的质量求出硫酸中溶质的质量,从而求出废液中硫酸的质量分数即可;
④根据铁钉的铁锈未除净,则铁锈消耗一部分硫酸进行解答.
解答:解:硝酸铵(NH4NO3)是一种常用的氮肥,其中氮、氢、氧三种元素的质量比为(14×2):(1×4):(16×3)=7:1:12.
配制200g溶质质量分数为5%的硝酸铵溶液,需要硝酸铵的质量为200g×5%=10g;需要水的质量为为:200g-10g=190g.
故答案为:7:1:12;10;190.
(2)①反应的化学方程式:Fe+H2SO4═FeSO4+H2↑;
②完全反应后,容器中的物质的质量差,就是生成氢气的质量,氢气的质量为:33.2g+10.8g-43.9g=0.1g;故填:0.1g;
③设与铁反应的硫酸的质量为x,
烧杯中稀硫酸废液的质量为:33.2g-18.2g=15.0g
Fe+H2SO4═FeSO4+H2↑
98 2
x 0.1g
=
X=4.9g
该废液中硫酸的质量分数为:
×100%=32.7%
答:废液中硫酸的质量分数是32.7%.
④如果铁钉的铁锈未除净,则铁锈消耗一部分硫酸,氧化铁和硫酸反应生成硫酸铁和水,反应方程式为Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;根据氢气求出的硫酸质量就偏小,从而使计算出的硫酸的质量分数偏小.
故填:偏小;铁锈也能消耗一部分硫酸.
配制200g溶质质量分数为5%的硝酸铵溶液,需要硝酸铵的质量为200g×5%=10g;需要水的质量为为:200g-10g=190g.
故答案为:7:1:12;10;190.
(2)①反应的化学方程式:Fe+H2SO4═FeSO4+H2↑;
②完全反应后,容器中的物质的质量差,就是生成氢气的质量,氢气的质量为:33.2g+10.8g-43.9g=0.1g;故填:0.1g;
③设与铁反应的硫酸的质量为x,
烧杯中稀硫酸废液的质量为:33.2g-18.2g=15.0g
Fe+H2SO4═FeSO4+H2↑
98 2
x 0.1g
| 98 |
| x |
| 2 |
| 0.1g |
X=4.9g
该废液中硫酸的质量分数为:
| 4.9g |
| 15.0g |
答:废液中硫酸的质量分数是32.7%.
④如果铁钉的铁锈未除净,则铁锈消耗一部分硫酸,氧化铁和硫酸反应生成硫酸铁和水,反应方程式为Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;根据氢气求出的硫酸质量就偏小,从而使计算出的硫酸的质量分数偏小.
故填:偏小;铁锈也能消耗一部分硫酸.
点评:本题主要考查化学方程式的书写和有关化学方程式的计算,难度较小,书写化学方程式时要注意四步,一是反应物和生成物的化学式要正确,二是遵循质量守恒定律,三是写上必要的条件,四是看是否有“↑”或“↓”.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
用分子的性质解释下列事实,错误的是( )
| A、事实:酒香不怕巷子深 解释:分子在不断地运动 |
| B、事实:氧化钠溶液具有导电性 解释:溶液中自由移动的离子 |
| C、事实:夏天湿衣服晾干快 解释:温度越高,分子运动速率越快 |
| D、事实:用乙烯合成聚乙烯塑料 解释:分子之间有间隔 |
为减缓化学反应速率,下列做法合理的是( )
| A、面团发酵时放在温热处 |
| B、在食品密封包装时充入氮气 |
| C、煤燃烧时向煤炉中鼓入空气 |
| D、用食醋除水垢时使用浓度高的食醋 |
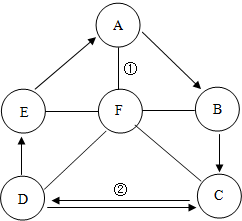 A~F均为初中所学的物质.其中属于碱的是B、C,属于盐的是D、E,其中D是钠盐;胃酸中含有F能帮助消化,A是食品包装袋中常用的干燥剂.其物质间的转化关系如图所示.图中“-”表示两端的物质能发生反应;“→”表示物质间存在转化关系,其余反应条件、部分反应物和生成物均已略去.试回答:
A~F均为初中所学的物质.其中属于碱的是B、C,属于盐的是D、E,其中D是钠盐;胃酸中含有F能帮助消化,A是食品包装袋中常用的干燥剂.其物质间的转化关系如图所示.图中“-”表示两端的物质能发生反应;“→”表示物质间存在转化关系,其余反应条件、部分反应物和生成物均已略去.试回答: