题目内容
某食盐样品中含有少量沙土、氯化钙和氯化镁以下是除去氯化钠样品中少量氯化钙和氯化镁的流程:
根据流程图回答:
(1)操作Ⅰ的名称是 ;
(2)加入过量NaOH的目的是除去氯化镁,反应的化学方程式为 ;
(3)加入的试剂A是 ,沉淀是 ;
(4)蒸发结晶时用到玻璃棒的作用是 .

根据流程图回答:
(1)操作Ⅰ的名称是
(2)加入过量NaOH的目的是除去氯化镁,反应的化学方程式为
(3)加入的试剂A是
(4)蒸发结晶时用到玻璃棒的作用是
考点:氯化钠与粗盐提纯,蒸发与蒸馏操作,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见的盐 化学肥料
分析:(1)根据不溶于液体的固体和液体分离的方法考虑;
(2)根据方程式的写法考虑;
(3)根据除杂质氯化钙的方法考虑;
(4)根据玻璃棒的用途考虑.
(2)根据方程式的写法考虑;
(3)根据除杂质氯化钙的方法考虑;
(4)根据玻璃棒的用途考虑.
解答:解:
(1)沙土不溶于水,可以通过过滤,将沙土与液体分离开;
(2)为了除去MgCl2,可以加入的试剂是氢氧化钠溶液;因此反应物是氢氧化钠和氯化镁,生成物是氢氧化镁沉淀和氯化钠反应的方程式为:2NaOH+MgCl2═Mg(OH)2↓+2NaCl;
(3)加入试剂A是为了除去氯化钙,由于碳酸钙是沉淀,有不能引入新的杂质,所以加入碳酸钠溶液就行,碳酸钠与氯化钙反应生成碳酸钙沉淀;
(4)蒸发结晶时用到玻璃棒的作用是搅拌,防止局部过热导致液滴飞溅.
故答案为:(1)过滤;
(2)2NaOH+MgCl2═Mg(OH)2↓+2NaCl;
(3)碳酸钠溶液;碳酸钙;
(4)防止局部过热导致液滴飞溅
(1)沙土不溶于水,可以通过过滤,将沙土与液体分离开;
(2)为了除去MgCl2,可以加入的试剂是氢氧化钠溶液;因此反应物是氢氧化钠和氯化镁,生成物是氢氧化镁沉淀和氯化钠反应的方程式为:2NaOH+MgCl2═Mg(OH)2↓+2NaCl;
(3)加入试剂A是为了除去氯化钙,由于碳酸钙是沉淀,有不能引入新的杂质,所以加入碳酸钠溶液就行,碳酸钠与氯化钙反应生成碳酸钙沉淀;
(4)蒸发结晶时用到玻璃棒的作用是搅拌,防止局部过热导致液滴飞溅.
故答案为:(1)过滤;
(2)2NaOH+MgCl2═Mg(OH)2↓+2NaCl;
(3)碳酸钠溶液;碳酸钙;
(4)防止局部过热导致液滴飞溅
点评:除杂质时加入的试剂只能与杂质反应,不能引入新的杂质,将不溶于液体的固体和液体分离用过滤的方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
已知两种物质发生化学反应的微观示意图如图(一种小球代表一种原子,原子间的短线代表原子的结合),下列说法不正确的是( )


| A、图示中共有3种化合物 |
| B、说明化学反应中原子不可分 |
| C、该反应符合质量守恒定律 |
| D、该反应属于置换反应 |
人类每年向地壳和海洋中索取大量的金属矿物资源,以提取数以吨计的金属.其中提取量最大的是( )
| A、铜 | B、铝 | C、铁 | D、银 |
很早的时候,人们将铅块压制成细长的铅条来写字,这就是最早的铅笔.下列有关铅的物理性质,不能据此得出的是( )
| A、铅的硬度较小 |
| B、铅具有良好的延展性 |
| C、铅条呈深灰色 |
| D、铅的密度较大 |
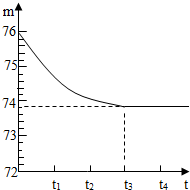 我省各地都有丰富的石灰石矿产资源.有一矿山上的石灰石样品,其中只含杂质二氧化硅(二氧化硅是一种既不溶于水也不与盐酸反应且耐高温的固体).小琳和他的同学想测定该样品中碳酸钙的质量分数,他们取一块石灰石样品,将其敲打粉碎后,称出6g放入烧杯内(烧杯的质量为20g),然后加入50g某一定溶质质量分数且足量的稀盐酸,用玻璃棒搅拌至不再产生气泡为止.反应所需时间(t)和烧杯及其所盛物质的总质量(m)的关系如图所示.试回答:
我省各地都有丰富的石灰石矿产资源.有一矿山上的石灰石样品,其中只含杂质二氧化硅(二氧化硅是一种既不溶于水也不与盐酸反应且耐高温的固体).小琳和他的同学想测定该样品中碳酸钙的质量分数,他们取一块石灰石样品,将其敲打粉碎后,称出6g放入烧杯内(烧杯的质量为20g),然后加入50g某一定溶质质量分数且足量的稀盐酸,用玻璃棒搅拌至不再产生气泡为止.反应所需时间(t)和烧杯及其所盛物质的总质量(m)的关系如图所示.试回答: