题目内容
15.水与人类生活和生产密切相关.请回答下列问题:(1)要除去水中不溶性杂质,要经过静置、沉淀、过滤等操作;
(2)要吸附水中的颜色和异味,可以用活性炭;
(3)生活中可以用肥皂水来区分硬水和软水;
(4)生活中常通过煮沸的方法降低水的硬度.
分析 (1)根据除去水中不溶性杂质常用的操作方法分析回答;
(2)根据活性炭具有吸附性分析回答;
(3)根据区分硬水和软水的方法分析回答;
(4)根据生活中降低水的硬度的方法分析回答.
解答 解:(1)过滤能将固液分开,要除去水中不溶性杂质,要经过静置、沉淀、过等操作;
(2)活性炭具有吸附性,要吸附水中的颜色和异味,可以用活性炭;
(3)生活中可以用 肥皂水来区分硬水和软水,遇肥皂水产生泡沫少的是硬水,遇肥皂水产生泡沫多的是软水;
(4)生活中常通过煮沸 的方法降低水的硬度.
故答为:(1)过滤;(2)活性炭;(3)肥皂水;(4)煮沸.
点评 本题难度不大,掌握水的净化原理与方法、硬水和软水的检验方法等是正确解答本题的关键.

练习册系列答案
相关题目
10.下列说法中正确的是( )
| A. | 氢气和氧气反应生成水,说明水是由氢、氧两种元素组成的 | |
| B. | 电解水生成氢气和氧气,说明水是由氢气和氧气组成的 | |
| C. | 河水经过过滤和活性炭吸附后得到的水是纯净物 | |
| D. | 水和过氧化氢的组成元素相同,所以化学性质也一样 |
20.下列有关合金的说法错误的是( )
| A. | 铝合金是一种化合物 | B. | 生铁是一种铁的合金 | ||
| C. | 黄铜的硬度比纯铜的硬度大 | D. | 焊锡的熔点比锡的熔点低 |
4. 为了测定某种黄铜(铜和锌的合金)的组成,现取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如下表:(Zn+H2SO4═H2↑+ZnSO4)
为了测定某种黄铜(铜和锌的合金)的组成,现取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如下表:(Zn+H2SO4═H2↑+ZnSO4)
(1)第2次测得剩余固体质量为74g,其成分中含铜、锌物质.
(2)该黄铜样品中铜和锌的质量比是27:13.
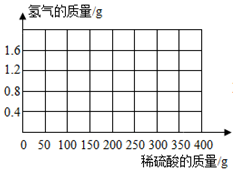
(3)计算所用稀硫酸的溶质质量分数,并画出反应生成的氢气质量与加入稀硫酸质量的关系图.
 为了测定某种黄铜(铜和锌的合金)的组成,现取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如下表:(Zn+H2SO4═H2↑+ZnSO4)
为了测定某种黄铜(铜和锌的合金)的组成,现取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如下表:(Zn+H2SO4═H2↑+ZnSO4)| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加人稀硫酸质量(g) | 100 | 100 | 100 | 100 |
| 剩余固体质量(g) | 87 | 74 | 67.5 | 67.5 |
(2)该黄铜样品中铜和锌的质量比是27:13.
(3)计算所用稀硫酸的溶质质量分数,并画出反应生成的氢气质量与加入稀硫酸质量的关系图.
5.下列除杂所用试剂和主要实验操作均正确的是( )
| 物质(括号内为杂质) | 所用试剂 | 主要实验操作 | |
| A | MnO2(KCl) | H2O | 溶解、过滤 |
| B | NaCl (MgSO4) | NaOH | 溶解、过滤、蒸发 |
| C | SO2(CO) | 盐酸 | 溶解、蒸发结晶 |
| D | NH3(H2O) | 浓H2SO4 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |


 ;(4)4个氢原子4H;
;(4)4个氢原子4H; 表示的是Cl-;(10)地壳中含量最多的金属元素Al.
表示的是Cl-;(10)地壳中含量最多的金属元素Al.