题目内容
15.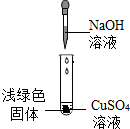 兴趣小组实验中,将NaOH溶液滴入CuSO4溶液中,结果溶液中生成了浅绿色的固体.于是,他们对该浅绿色固体的成分进行探究.
兴趣小组实验中,将NaOH溶液滴入CuSO4溶液中,结果溶液中生成了浅绿色的固体.于是,他们对该浅绿色固体的成分进行探究.【查阅资料】
①NaOH与CuSO4反应会生产Cu(OH)2,也会生成Cu4(OH)4SO4(碱式硫酸铜).
②Cu(OH)2在80℃会分解生成CuO.
③Cu4(OH)4SO4不溶于水,能与酸反应,分解温度需300℃.
【猜想与假设】
猜想一:浅绿色固体为Cu(OH)2.
猜想二:浅绿色固体为Cu4(OH)4SO4.
猜想三:浅绿色固体为Cu(OH)2和Cu4(OH)4SO4.
【获取事实与证据】
①取少量浅绿色固体放入试管中,加热至100℃,观察到黑色固体物质,说明浅绿色固体中存在氢氧化铜.
②另取少量浅绿色固体放入试管中,加入足量稀硝酸,再滴加Ba(NO3)2溶液,出现白色沉淀,该白色沉淀是硫酸钡.
【结论】整个实验证明猜想③正确.
分析 【猜想与假设】根据题意,NaOH与CuSO4反应会生成Cu(OH)2,也会生成Cu4(OH)4SO4(碱式硫酸铜),则浅绿色固体可能为Cu(OH)2,也可能是Cu4(OH)4SO4,也可能是两者的混合物.
【获取事实与证据】①根据题意,Cu(OH)2在80℃会分解生成CuO,Cu4(OH)4SO4不溶于水,能与酸反应,分解温度需300℃,进行分析解答.
②由题意,另取少量浅绿色固体放入试管中,加入足量稀硝酸,再滴加Ba(NO3)2溶液,出现白色沉淀,说明生成了不溶于酸的硫酸钡沉淀,进行分析解答.
解答 【猜想与假设】由题意,NaOH与CuSO4反应会生成Cu(OH)2,也会生成Cu4(OH)4SO4(碱式硫酸铜).
【获取事实与证据】①由题意,Cu(OH)2在80℃会分解生成CuO,而Cu4(OH)4SO4不溶于水,能与酸反应,分解温度需300℃.取少量浅绿色固体放入试管中,加热至100℃,此温度下Cu4(OH)4SO4还没分解,观察到黑色固体物质,说明浅绿色固体中存在氢氧化铜,黑色固体物质是氢氧化铜分解生成的.
②Cu4(OH)4SO4不溶于水,能与酸反应,另取少量浅绿色固体放入试管中,加入足量稀硝酸,再滴加Ba(NO3)2溶液,出现白色沉淀,说明生成了硫酸钡白色沉淀,则说明浅绿色固体中存在Cu4(OH)4SO4.
【结论】由事实与证据,浅绿色固体中含有Cu(OH)2、Cu4(OH)4SO4,整个实验证明猜想③正确.
故答案为:【猜想与假设】Cu4(OH)4SO4;
【获取事实与证据】①氢氧化铜;②硫酸钡;
【结论】③.
点评 本题难度不大,理解NaOH与CuSO4反应会生成Cu(OH)2和Cu4(OH)4SO4、Cu4(OH)4SO4能与酸反应,掌握酸的化学性质并能灵活运用是正确解答本题的关键.

 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案| A. | 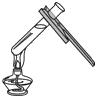 给试管内液体加热 | B. |  取用块状固体 | ||
| C. | 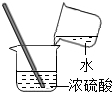 稀释浓硫酸 | D. | 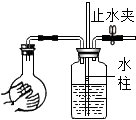 气密性检查 |
| A. | 水是一种常见的溶剂 | B. | 长期饮用蒸馏水不利于人体健康 | ||
| C. | 加热煮沸将硬水转化为软水 | D. | 过滤能除去天然水中所有的杂质 |
| A. | 青蒿素是由碳、氢、氧三种元素组成的有机物 | |
| B. | 青蒿素分子中C、H、O三种元素的质量比为12:1:16 | |
| C. | 青蒿素中氢元素质量分数的计算式是$\frac{22}{281}$×100% | |
| D. | 青蒿素分子是由15个碳原子11个氢原子和5个氧原子构成的 |
| A. | 活性炭可除去水中的异味 | B. | 过滤可以除去水中所有的杂质 | ||
| C. | 硬水通过煮沸可降低硬度 | D. | 蒸馏对水的净化程度最高 |
| A. |  | B. | 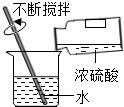 | C. |  | D. | 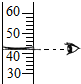 |
| A. | 酒中含有的酒精属于有机物 | B. | K2Cr2O7属于氧化物 | ||
| C. | K2Cr2O7中铬元素的化合价为+6价 | D. | 硫酸铬的化学式为Cr2(SO4)3 |
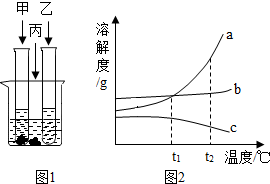 在室温下,甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,充分溶解后现象如图1所示.升温到90℃时,发现甲固体全部溶解,丙固体明显增多,另一试管中无明显现象.
在室温下,甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,充分溶解后现象如图1所示.升温到90℃时,发现甲固体全部溶解,丙固体明显增多,另一试管中无明显现象.