题目内容
一定量的铜锌合金样品与80g溶质质量分数为24.5%的稀硫酸恰好完全反应(Zn+H2SO4═ZnSO4+H2↑)
(1)将上述稀硫酸80g加水稀释至200g,所得溶液溶质的质量分数是: .
(2)计算样品中的锌量?
(1)将上述稀硫酸80g加水稀释至200g,所得溶液溶质的质量分数是:
(2)计算样品中的锌量?
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据稀释前后溶质的质量不变,利用溶质质量分数计算公式来解决;
(2)根据锌与硫酸反应的化学方程式利用硫酸的质量计算锌的质量.
(2)根据锌与硫酸反应的化学方程式利用硫酸的质量计算锌的质量.
解答:解:(1)根据稀释前后溶质的质量不变,所得溶液溶质的质量分数=
×100%=
×100%=9.8%
故答案为:9.8%;
(2)设样品中锌的质量为x
Zn+H2SO4=H2↑+ZnSO4
65 98
x 80g×24.5%
=
解得:x=13g
答:样品中锌的质量为13g.
| 溶质的质量 |
| 溶液的质量 |
| 80g×24.5% |
| 200g |
故答案为:9.8%;
(2)设样品中锌的质量为x
Zn+H2SO4=H2↑+ZnSO4
65 98
x 80g×24.5%
| 65 |
| 98 |
| x |
| 80g×24.5% |
解得:x=13g
答:样品中锌的质量为13g.
点评:注意稀释前后溶质的质量不变.

练习册系列答案
相关题目
2012年6月16日,“神舟”九号飞船在酒泉发射中心升空.并和“天宫“一号自动交会对接,这次飞行使用的燃料中有液氢和液氧.下列与此相关的说法中不正确的是( )
| A、液氢燃烧时化学能转化为热能 |
| B、液氢和液氧都是化合物 |
| C、液氧的作用是支持液氢燃烧 |
| D、液氢作燃料能减轻发射质量 |
依据如图所示,下列说法中不正确的是( )
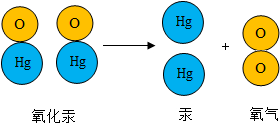

| A、原子不能直接构成物质 |
| B、化学变化中原子不能再分 |
| C、该反应属于分解反应 |
| D、氧分子保持氧气的化学性质 |
 如图是初中化学中常见的物质之间的转化关系,其中甲、乙、丙为单质;A,B,C,D,E为化合物,且A与B的组成元素相同,D与E的组成元素也相同.已知C、丙均为黑色粉末,C和E在高温条件下可生成丙和D,D能使澄清石灰水变浑浊.其余反应条件及部分反应物和生成物均已略去.
如图是初中化学中常见的物质之间的转化关系,其中甲、乙、丙为单质;A,B,C,D,E为化合物,且A与B的组成元素相同,D与E的组成元素也相同.已知C、丙均为黑色粉末,C和E在高温条件下可生成丙和D,D能使澄清石灰水变浑浊.其余反应条件及部分反应物和生成物均已略去.
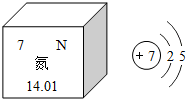 氮在周期表中的信息和原子结构示意图如图.根据信息,氮元素的相对原子质量为
氮在周期表中的信息和原子结构示意图如图.根据信息,氮元素的相对原子质量为