题目内容
5.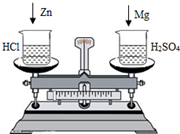 在托盘天平的两边各放一只等质量的烧杯,向两只烧杯中分别注入相同质量、相同质量分数的盐酸和稀硫酸,天平平衡若向左边烧杯中投入少量的锌粒,向右边烧杯中投入等质量的镁条(如图所示),待充分反应后,发现锌粒和镁条均有剩余,则天平指针( )
在托盘天平的两边各放一只等质量的烧杯,向两只烧杯中分别注入相同质量、相同质量分数的盐酸和稀硫酸,天平平衡若向左边烧杯中投入少量的锌粒,向右边烧杯中投入等质量的镁条(如图所示),待充分反应后,发现锌粒和镁条均有剩余,则天平指针( )| A. | 先向右偏,后向左偏 | B. | 先向左偏,后向右偏 | ||
| C. | 一直向左偏 | D. | 一直向右偏 |
分析 根据金属与酸反应的化学方程式进行计算,可以从金属足量的角度进行分析完成.
解答 解:两烧杯中锌粒和镁条均有剩余,则酸全部参加反应,设酸的质量是98,盐酸反应生成的氢气的质量为x,
Zn+2HCl═ZnCl2+H2↑
73 2
98 x
$\frac{73}{98}=\frac{2}{x}$
x=2.7
硫酸反应生成的氢气的质量为y,
Mg+H2SO4═MgSO4+H2↑
98 2
98 y
$\frac{98}{98}=\frac{2}{y}$
y=2
可以看出盐酸生成的氢气质量比硫酸生成的氢气的质量多,故天平指针最终会指向硫酸一端.
但是由于镁比锌活泼,且盐酸和硫酸中氢离子浓度差别不是很大,而镁是镁条,锌为锌粒,所以应该是镁条反应明显比锌粒快,所以镁开始生成氢气速度比锌粒快,导致开始向盐酸一侧倾斜.
所以应该是先向左倾斜,后指向右侧.
答案为:B.
点评 本题考查了金属与酸反应生成氢气质量的关系,完成此题,可以依据反应的化学方程式,从酸的质量和金属的质量的角度进行.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
7.下列有关实验现象的描述,正确的是( )
| A. | 镁条在空气中燃烧发出蓝紫色火焰,产生大量白烟 | |
| B. | 电解水正极一侧得到的气体能使带火星的木条复燃 | |
| C. | 细铁丝在氧气中燃烧,火星四射,生成红棕色固体 | |
| D. | 打开浓硫酸的试剂瓶盖时,瓶口有白雾产生 |
5.下列说法正确的是( )
| A. | 油锅着火立即用冷水浇灭 | |
| B. | 向土壤里撒熟石灰,可改良碱性土壤 | |
| C. | 用汽油能除去衣服上的油污是利用乳化原理 | |
| D. | 钢铁在潮湿的环境中比在干燥的环境中更容易被腐蚀 |
12.碳酸钾和碳酸钙的固体混合物75g与足量的稀盐酸充分反应后,如果将反应后的溶液蒸干得到82.7g固体,则原混合物中金属元素的质量分数为( )
| A. | 40% | B. | 44% | C. | 48% | D. | 52% |
10.如图,为探究CO2和NaOH确实发生了化学反应,某实验小组的同学设计出了如下实验装置,请回答下列问题:
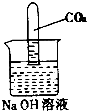
(1)请简述出现的实验现象试管内液面上升,烧杯内液面下降,产生该实验现象的原因是:NaOH与CO2发生反应生成碳酸钠和水,使容器内气压变小,产生气压差.
(2)某同学质疑(1)实验设计,该同学质疑的依据是:二氧化碳与氢氧化钠反应后试管和软塑料瓶内压强变小,二氧化碳能溶于水,且与水反应后也会使试管和软塑料瓶内压强变小.
(3)在原实验的基础上,请你设计实验证明CO2和NaOH肯定发生了化学反应.

(1)请简述出现的实验现象试管内液面上升,烧杯内液面下降,产生该实验现象的原因是:NaOH与CO2发生反应生成碳酸钠和水,使容器内气压变小,产生气压差.
(2)某同学质疑(1)实验设计,该同学质疑的依据是:二氧化碳与氢氧化钠反应后试管和软塑料瓶内压强变小,二氧化碳能溶于水,且与水反应后也会使试管和软塑料瓶内压强变小.
(3)在原实验的基础上,请你设计实验证明CO2和NaOH肯定发生了化学反应.
| 实验步骤 | 实验现象 | 实验结论 |
| 取反应后的溶液滴入稀盐酸, | 若有大量气泡产生 | 可以肯定二氧化碳与氢氧化钠发生了反应 |
14.控制变量法是实验探究的重要方法.利用如图所示实验不能实现的探究目的是( )


| A. | 甲中①②对比可探究铁的锈蚀与水是否有关 | |
| B. | 甲中①③对比可探究铁的锈蚀与植物油是否有关 | |
| C. | 乙可探究可燃物的燃烧足否需要与氧气接触 | |
| D. | 乙可探究可燃物的燃烧是否需要达到一定温度 |
15.下列过程中没有化学变化的是( )
| A. | CO2溶于水 | B. | 钢铁生锈 | ||
| C. | 干冰升华 | D. | 蛋壳中加入稀盐酸 |
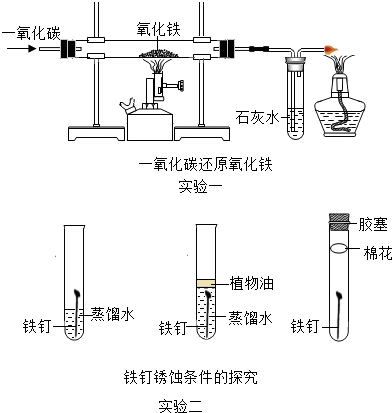 初中化学教材中的一些实验如图所示,请你回答下列问题:
初中化学教材中的一些实验如图所示,请你回答下列问题: 铁锅、铝锅是生活中常用的炊具,如图是铁锅的示意图.
铁锅、铝锅是生活中常用的炊具,如图是铁锅的示意图.