题目内容
 使用如图所示装置测定空气中氧气的含量,请回答:
使用如图所示装置测定空气中氧气的含量,请回答:
(1)为确保实验成功,实验前一定要检验装置的______
(2)在______(填装置名称)中添加红磷的量应该______(填“随意”、“过量”或“少量”)
(3)写出红磷燃烧时的化学方程式______,此时可以观察到的现象是______.燃烧停止,待冷却后打开弹簧夹.
(4)该实验最终得到的结论是______.
解:(1)如果装置漏气,会使装置内外压强相等,水不会被压入瓶内;
(2)红磷量不足不能把装置内氧气消耗完,导致进入得水偏少,会得出错误结论;
(3)写出红磷燃烧时的化学方程式 4P+5O2 2P2O5,此时可以观察到的现象是 发出黄光,放出热量,冒出大量的白烟.
2P2O5,此时可以观察到的现象是 发出黄光,放出热量,冒出大量的白烟.
(4)进入的水的体积就是被消耗的氧气的体积,所以说明空气中氧气约占空气体积的五分之一.
故答案为:(1)气密性;(2)燃烧匙,过量;(3)4P+5O2 2P2O5
2P2O5
发出黄光,放出热量,冒出大量的白烟.(4)空气中氧气约占空气体积的五分之一.
分析:根据测定空气中氧气的含量的步骤、现象结合压强的知识分析.本题根据漏气和红磷量不足导致的结果考虑;根据红磷燃烧的现象和消耗氧气后由于压强减小导致的现象考虑;根据实验现象考虑实验结论.
点评:解答本题关键是要知道装置必须密封,为了把氧气消耗完,必须加入过量的红磷.知道进入水的体积就是消耗的氧气的体积.
(2)红磷量不足不能把装置内氧气消耗完,导致进入得水偏少,会得出错误结论;
(3)写出红磷燃烧时的化学方程式 4P+5O2
 2P2O5,此时可以观察到的现象是 发出黄光,放出热量,冒出大量的白烟.
2P2O5,此时可以观察到的现象是 发出黄光,放出热量,冒出大量的白烟.(4)进入的水的体积就是被消耗的氧气的体积,所以说明空气中氧气约占空气体积的五分之一.
故答案为:(1)气密性;(2)燃烧匙,过量;(3)4P+5O2
 2P2O5
2P2O5发出黄光,放出热量,冒出大量的白烟.(4)空气中氧气约占空气体积的五分之一.
分析:根据测定空气中氧气的含量的步骤、现象结合压强的知识分析.本题根据漏气和红磷量不足导致的结果考虑;根据红磷燃烧的现象和消耗氧气后由于压强减小导致的现象考虑;根据实验现象考虑实验结论.
点评:解答本题关键是要知道装置必须密封,为了把氧气消耗完,必须加入过量的红磷.知道进入水的体积就是消耗的氧气的体积.

练习册系列答案
相关题目
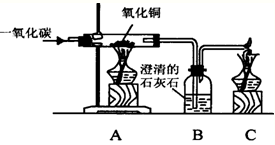 某同学使用如图所示装置,试验一氧化碳与氧化铜的反应.请回答下列有关问题:
某同学使用如图所示装置,试验一氧化碳与氧化铜的反应.请回答下列有关问题: 某化学小组利用如图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去)探究过程如下:
某化学小组利用如图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去)探究过程如下: 使用如图所示装置测定空气中氧气的含量,请回答:
使用如图所示装置测定空气中氧气的含量,请回答: 某同学利用如图所示装置测定空气中氧气的含量,先用弹簧夹夹住橡皮管,点燃红磷,伸入瓶中并塞上瓶塞.等红磷燃烧熄灭后再打开弹簧夹,发现集气瓶中的水少于其容积的
某同学利用如图所示装置测定空气中氧气的含量,先用弹簧夹夹住橡皮管,点燃红磷,伸入瓶中并塞上瓶塞.等红磷燃烧熄灭后再打开弹簧夹,发现集气瓶中的水少于其容积的