题目内容
(2006?成都)某工厂化验室用10%的氢氧化钠溶液洗涤定量石油产品中残余的硫酸,洗涤后溶液呈中性,共消耗这种氢氧化钠溶液40g.求在这一定量的石油产品里残余H2SO4的质量.
【答案】分析:由氢氧化钠溶液的质量和质量分数,根据氢氧化钠与硫酸反应的化学方程式可以计算出一定量石油产品里残余硫酸的质量.
解答:解:设残余硫酸的质量为x.
2NaOH+H2SO4=Na2SO4+2H2O
80 98
40g×10% x
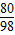 =
=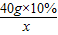 ,x=4.9g
,x=4.9g
答:在这一定量的石油产品里残余硫酸的质量4.9.
点评:本题主要考查含杂质物质的化学方程式计算和溶质质量分数的计算,难度稍大.
解答:解:设残余硫酸的质量为x.
2NaOH+H2SO4=Na2SO4+2H2O
80 98
40g×10% x
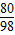 =
=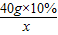 ,x=4.9g
,x=4.9g答:在这一定量的石油产品里残余硫酸的质量4.9.
点评:本题主要考查含杂质物质的化学方程式计算和溶质质量分数的计算,难度稍大.

练习册系列答案
相关题目

 (2006?成都)某实验中两组在用下图甲和乙装置做木炭还原氧化铜的实验中,发现从乙装置的导气管口不断有气泡逸出,以为是反应产生的CO2未被石灰水完全吸收.于是在乙装置后又连接上丙装置,重新实验,发现丙装置中仍不断有气泡逸出,且石灰水未见浑浊.那么从丙装置中逸出的气体是什么呢?请完成下列探究中的相关问题.
(2006?成都)某实验中两组在用下图甲和乙装置做木炭还原氧化铜的实验中,发现从乙装置的导气管口不断有气泡逸出,以为是反应产生的CO2未被石灰水完全吸收.于是在乙装置后又连接上丙装置,重新实验,发现丙装置中仍不断有气泡逸出,且石灰水未见浑浊.那么从丙装置中逸出的气体是什么呢?请完成下列探究中的相关问题.