题目内容
硫酸亚铁(FeSO4)可用于治疗缺铁性贫血,根据硫酸亚铁的化学式计算:
(1)硫酸亚铁中铁元素的质量分数
(2)某贫血患者需补充7g铁,至少需要多少克硫酸亚铁(结果保留一位小数).
(1)硫酸亚铁中铁元素的质量分数
(2)某贫血患者需补充7g铁,至少需要多少克硫酸亚铁(结果保留一位小数).
考点:元素的质量分数计算,化合物中某元素的质量计算
专题:化学式的计算
分析:根据硫酸亚铁的化学式为FeSO4,利用相对原子质量来计算元素的质量比、元素的质量分数,再根据需要的铁的质量及铁的质量分数来计算硫酸亚铁的质量.
解答:解:(1)由硫酸亚铁的化学式为FeSO4,则硫酸亚铁中铁元素的质量分数为
×100%=36.8%,故答案为:36.8%;
(2)由补充7g铁,铁元素的质量分数为
×100%,则硫酸亚铁的质量为7g÷
×100%=19g,答:至少需要19克硫酸亚铁.
故答案为:(1)36.8%;(2)19g
| 56 |
| 56+32+16×4 |
(2)由补充7g铁,铁元素的质量分数为
| 56 |
| 56+32+16×4 |
| 56 |
| 56+32+16×4 |
故答案为:(1)36.8%;(2)19g
点评:本题考查学生利用化学式的进行简单计算,学生熟悉原子的相对原子质量、元素质量比及元素质量分数的计算方法即可解答.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
如下粒子结构示意图得出的结论中,错误的是( )
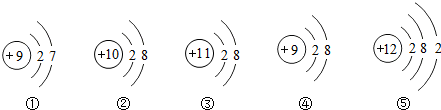

| A、①④属于同种元素 |
| B、②③④属于离子 |
| C、⑤易失去成为阴离子 |
| D、①⑤的结构不稳定 |
下列化学方程式书写正确的是( )
A、Fe+O2
| ||||
| B、CO+CuO═Cu+CO2 | ||||
| C、2H2O2═2H2+O2 | ||||
D、2Mg+O2
|
某同学称量固体药品时,误将砝码放在左盘,药品放于右盘,天平平衡后,共加砝码25g,游码处于0.5g处,则此固体药品的实际质量为( )
| A、25.5g | B、25g |
| C、24.5g | D、26g |
元素的化学性质主要决定于其原子的( )
| A、核内质子数 | B、中子数 |
| C、核外电子数 | D、最外层电子数 |