题目内容
实验是化学的灵魂,是学好化学的重要方法.

(1)实验甲的实验目的是探究碳的 性;实验乙观察到纸花变红,能否得出水能与二氧化碳反应的实验结论? ;实验丙观察到气球B的变化情况为 .
(2)《酸、碱的化学性质》实验中,向两支试管中各加入相同量的氢氧化钙粉末,然后各加入1mL水,振荡,再滴入1~2滴酚酞试液.继续向其中一支试管中加入1mL盐酸,向另一支中继续加1mL水,观察现象.以上实验得出氢氧化钙的化学性质有 ,继续加1mL水的目的是 ;要得出氢氧化钙微溶于水的实验结论,实验中取用氢氧化钙时要做到 .

(1)实验甲的实验目的是探究碳的
(2)《酸、碱的化学性质》实验中,向两支试管中各加入相同量的氢氧化钙粉末,然后各加入1mL水,振荡,再滴入1~2滴酚酞试液.继续向其中一支试管中加入1mL盐酸,向另一支中继续加1mL水,观察现象.以上实验得出氢氧化钙的化学性质有
考点:碳的化学性质,二氧化碳的化学性质,碱的化学性质,燃烧与燃烧的条件
专题:实验性简答题
分析:(1)根据实验测得装置、发生的反应分析回答有关的问题.
(2)氢氧化钙的水溶液呈碱性,能使酚酞试液变红;酸和碱能发生中和反应,酚酞在中性和酸性溶液中不变色,据此解答.
(2)氢氧化钙的水溶液呈碱性,能使酚酞试液变红;酸和碱能发生中和反应,酚酞在中性和酸性溶液中不变色,据此解答.
解答:解:(1)实验甲中,在高温条件下碳与氧化铜生成了铜和二氧化碳,通过该实验探究了碳的还原性;由于集气瓶中含有二氧化碳,实验乙根据纸花变红,不能得出水能与二氧化碳反应,可能是二氧化碳使纸花变红;由于白磷燃烧消耗了氧气,生成了五氧化二磷,放出大量的热,所以,实验丙观察到气球B的变化情况为:先变大,后缩小.
(2)《酸、碱的化学性质》实验中,向两支试管中各加入相同量的氢氧化钙粉末,然后各加入1mL水,振荡,再滴入1~2滴酚酞试液.继续向其中一支试管中加入1mL盐酸,向另一支中继续加1mL水.由加入的盐酸后溶液澄清了,可得出氢氧化钙能与盐酸反应,氢氧化钙具有的与酸反应化学性质,继续加1mL水的目的是对比;要得出氢氧化钙微溶于水的实验结论,实验中取用氢氧化钙时要做到少量.
故答为:(1)还原,不能,先变大,后缩小;(2)与酸反应的性质,对比,要少量.
(2)《酸、碱的化学性质》实验中,向两支试管中各加入相同量的氢氧化钙粉末,然后各加入1mL水,振荡,再滴入1~2滴酚酞试液.继续向其中一支试管中加入1mL盐酸,向另一支中继续加1mL水.由加入的盐酸后溶液澄清了,可得出氢氧化钙能与盐酸反应,氢氧化钙具有的与酸反应化学性质,继续加1mL水的目的是对比;要得出氢氧化钙微溶于水的实验结论,实验中取用氢氧化钙时要做到少量.
故答为:(1)还原,不能,先变大,后缩小;(2)与酸反应的性质,对比,要少量.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
如图是某化学反应的微观示意图.据图分析,下列说法错误的是( )


| A、该反应为化合反应 |
| B、反应物中有一种是单质 |
| C、原子是化学变化中的最小粒子 |
| D、所有元素的化合价在化学反应前后均不变 |
 某粒子的结构示意图如图,下列各粒子与该粒子处于同一主族且化学性质相似的是( )
某粒子的结构示意图如图,下列各粒子与该粒子处于同一主族且化学性质相似的是( )





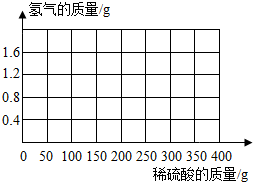 为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如表:
为了测定某种黄铜(铜和锌的合金)的组成,取该黄铜样品碎屑100g,把400g稀硫酸分4次加入到该样品中,测得数据记录如表: