题目内容
在化学实验室中,对某种化合物的溶液进行了以下实验:
① 取少量该溶液加入适量K2SO4溶液,产生白色沉淀,再加入稀硝酸,沉淀不溶解。
② 另取少量该溶液加入适量AgNO3溶液,产生白色沉淀,再加入稀硝酸,沉淀不溶解。则溶液中的物质一定是
A.BaCl2 B.CuCl2 C.Na2CO3 D.Ba(NO3)2
【答案】
A
【解析】
试题分析:根据所有的钾盐都会溶于水,不溶于硝酸的白色沉淀有氯化银、硫酸钡进行分析;所有的钾盐都会溶于水,加入硫酸钾后生成了不溶于硝酸的白色沉淀只能是硫酸钡,所以原化合物提供了钡离子;加入硝酸银也出现了不溶于硝酸的白色沉淀,只能是氯化银沉淀,所以原溶液提供了氯离子,故选A
考点:常见离子的检验方法及现象

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在化学实验室,某研究性学习小组发现了一个不和谐的音符,一瓶久置的氢氧化钠固体敞口露置在空气中,他们认为氢氧化钠固体可能变质了,为此他们展开了探究,请你参与.
【查阅资料】Ba(NO3)2溶液呈中性,碳酸钠溶液呈碱性
【实验猜想】可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
【实验探究】(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的Ba(NO3)2溶液,产生白色沉淀,静置后取上层清液,再滴入无色酚酞溶液,溶液变红色.根据实验现象,可确定该固体是 ;
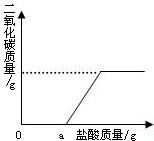
(2)再取固体样品溶于水,加入一定质量分数的稀硫酸,直至过量.测出加入稀硫酸的质量与产生CO2气体的质量关系如图所示.从图中可以判断:在该样品溶液中加入稀硫酸,首先与之反应的物质是 .
【实验分析】请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀硫酸反应,变质前消耗硫酸的质量 变质后消耗硫酸的质量(填“大于”、“小于”或“等于”).
【综合计算】(1)称取26.5g 该固体样品于锥形瓶中,加入一定质量分数的稀硫酸,直至过量,得到数据如下表:
根据二氧化碳的质量列出求解碳酸钠质量(x)的比例式为
(2)该固体样品中碳酸钠的质量分数是 .
【查阅资料】Ba(NO3)2溶液呈中性,碳酸钠溶液呈碱性
【实验猜想】可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
【实验探究】(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的Ba(NO3)2溶液,产生白色沉淀,静置后取上层清液,再滴入无色酚酞溶液,溶液变红色.根据实验现象,可确定该固体是
(2)再取固体样品溶于水,加入一定质量分数的稀硫酸,直至过量.测出加入稀硫酸的质量与产生CO2气体的质量关系如图所示.从图中可以判断:在该样品溶液中加入稀硫酸,首先与之反应的物质是

【实验分析】请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀硫酸反应,变质前消耗硫酸的质量
【综合计算】(1)称取26.5g 该固体样品于锥形瓶中,加入一定质量分数的稀硫酸,直至过量,得到数据如下表:
| 样品质量 | 反应前总质量 | 反应后总质量 |
| 26.5克 | 148.5克 | 146.3克 |
(2)该固体样品中碳酸钠的质量分数是
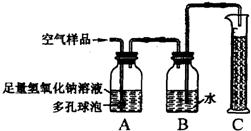 22、据报道,从2005年1月1日起,贵州省各地环保部门将对实验室类污染实施严格的环境监管.由于学校化学实验室要排放成分复杂的污染物,所以也被列为环境监管范围.某校化学兴趣小组的同学在甲实验室中进行了氧气分别与碳、硫、铁反应的实验后,为了解该实验产生的气体对空气成分造成的影响,接着设计了如下实验装置进行实验(图中多孔球泡的作用是:增大气体与溶液的接触面积,使反应充分进行).
22、据报道,从2005年1月1日起,贵州省各地环保部门将对实验室类污染实施严格的环境监管.由于学校化学实验室要排放成分复杂的污染物,所以也被列为环境监管范围.某校化学兴趣小组的同学在甲实验室中进行了氧气分别与碳、硫、铁反应的实验后,为了解该实验产生的气体对空气成分造成的影响,接着设计了如下实验装置进行实验(图中多孔球泡的作用是:增大气体与溶液的接触面积,使反应充分进行).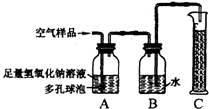 某校化学兴趣小组的同学在甲实验室中进行了氧气分别与碳、硫、铁反应的实验后,为了解该实验产生的气体对空气成分造成的影响,接着设计了如下实验装置进行实验(图中多孔球泡的作用是:增大气体与溶液的接触面积,使反应充分进行).
某校化学兴趣小组的同学在甲实验室中进行了氧气分别与碳、硫、铁反应的实验后,为了解该实验产生的气体对空气成分造成的影响,接着设计了如下实验装置进行实验(图中多孔球泡的作用是:增大气体与溶液的接触面积,使反应充分进行).