题目内容
12.某研究性学习小组欲利用下列装置进行相关气体制取的探究,请你分析并填空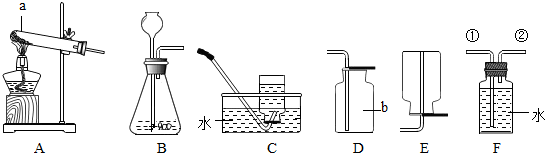
(1)写出图中仪器a名称试管.
(2)实验室制取二氧化碳的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑.应选择的气体发生装置是B,气体收集装置是D(填序号).
(3)实验室加热氯酸钾和二氧化锰制取氧气的化学方程式是2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,该反应为分解反应(填反应类型). 若用盛满水的F装置收集氧气,应从导管②(填①或②)通入.
(4)甲烷是一种无色、无味、难溶于水、密度小于空气密度的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,则实验室制取并收集甲烷应选择的装置组合是AC或AE.
分析 (1)熟记仪器的名称;
(2)实验室常用石灰石(或大理石)与稀盐酸反应制取二氧化碳,据此写出化学反应式.根据实验室中制取二氧化碳的反应原理和反应条件来选择反应的发生装置,根据二氧化碳的密度及水溶性来选择收集装置.
(3)根据氯酸钾在一定条件下分解为氯化钾和氧气书写化学反应方程式;从F装置相当于排水法收集氧气考虑;
(4)根据实验室制取甲烷的反应原理和甲烷的性质选择所需装置.
解答 解:(1)a是试管,故填:试管;
(2)实验室常用石灰石(或大理石)与稀盐酸反应制取二氧化碳,反应的化学反应式是:CaCO3+2HCl=CaCl2+H2O+CO2↑.在实验室中制取二氧化碳常用石灰石(或大理石)和稀盐酸反应来制取,属于固液常温型,所以应该选择装置B来制取二氧化碳气体;二氧化碳密度比空气大,能溶于水,所以应该选择装置D来收集二氧化碳.故填:CaCO3+2HCl=CaCl2+H2O+CO2↑;B;D;
(3)实验室加热氯酸钾和二氧化锰制取氧气的化学方程式是:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑,符合“一变多”的特征,属于分解反应;用盛满水的F装置收集氧气,相当于排水法收集氧气,气体可从②进入,水被从①排出;
故答案为:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;A;②;
(4)实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷,属于“固固加热型”,所以应选择的发生装置为 A,甲烷密度小于空气,难溶于水,可选择向下排空气法或排水法收集,所以选择收集装置为C或E.故填:AC或AE.
点评 本题难度很大,是中考的重要考点之一,熟练掌握实验室中制取气体的反应原理、发生装置和收集装置的选择依据是正确解答本题的关键.

| A. | 蒸馏水 | B. | 氢氧化钠 | C. | 空气 | D. | 氧气 |
| 相关化学知识、说法 | 解释 | |
| A | 碳、硫与氧气反应是化合反应 | 氧气均支持这些物质燃烧 |
| B | 氧化钙和浓硫酸加入水都放热 | 二者均发生了化学变化 |
| C | 稀硫酸、硫酸铜溶液显酸性 | 溶液中均含有硫酸酸根离子 |
| D | 乙醇和甲烷都是有机物 | 二者均为碳元素的化合物 |
| A. | A | B. | B | C. | C | D. | D |
【提出问题】
刚出窑的“石灰”有那些成分?
【猜想】
I.只有氧化钙Ⅱ.只有碳酸钙ⅢI.既有氧化钙也有碳酸钙
【实验探究】
(1)甲同学从样品中取一定量的固体于试管中,并加入一定量的水,振荡,有白色不溶物.甲同学据此认为试管中的固体为碳酸钙,即猜想 II成立.乙同学认为上述实验不足以证明猜想 II成立,其理由是沉淀也可能是未溶解的氢氧化钙,有白色不溶物只能说明样品可能有碳酸钙,不能说明 II.只有碳酸钙.
(2)乙同学从样品中取一定量的固体于试管中,加入一定量的水,触摸试管外壁,感觉发热;继续向试管中加入几滴稀盐酸,没有发现气泡产生.乙同学据此认为试管中的固体只有氧化钙,即猜想I成立.丙同学认为乙的实验不足以证明猜想I成立,理由是滴加的稀盐酸不足量,几滴稀盐酸和氢氧化钙反应,没有和碳酸钙反应.
(3)丙同学认为利用感觉温度变化的方法判断是否有氧化钙不可靠,他用水、酚酞试液和稀盐酸证明了猜想Ⅲ成立,请完成他的实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取样品加水溶解滴加酚酞 ②取样品滴加稀盐酸 | 溶液变红 有气泡产生 | 猜想Ⅲ成立 |
| A. | 纸张燃烧 | B. | 花香四溢 | C. | 灯泡发光 | D. | 滴水成冰 |
| A. |  | B. | 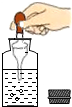 | C. | 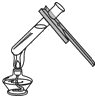 | D. |  |
| 第一次 | 第二次 | 第三次 | |
| 所取合金的质量/g | 25 | 25 | 50 |
| 所用稀硫酸的质量/g | 120 | 160 | 100 |
| 生成氢气的质量/g | 0.4 | 0.4 | 0.4 |
②试计算该铜锌合金中锌的质量分数(写出计算过程).52%
③从上表数据分析,当所取合金与所用稀硫酸的质量比为1:4时,表明合金中的锌与稀硫酸中的硫酸恰好完全反应.
 如图所示A--F是初中化学常见的物质.图中“→”表示转化关系,“-“表示相互能反应(部分物质和反应条件未标出).其中A是紫红色金属,B常温下是气体,C是人体胃液中含有的酸.
如图所示A--F是初中化学常见的物质.图中“→”表示转化关系,“-“表示相互能反应(部分物质和反应条件未标出).其中A是紫红色金属,B常温下是气体,C是人体胃液中含有的酸.