题目内容
10.请你根据如图来回答有关问题:
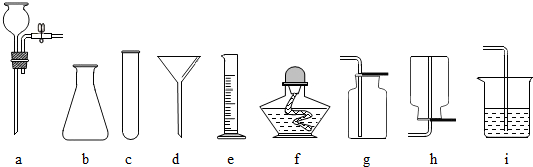
(1)写出有标号的仪器名称a酒精灯、b长颈漏斗.
(2)在加入药品之前应对装置进行检查装置的气密性.
(3)可用于实验室制备和收集O2的一套装置是(填字母编号)BC或BE.写出用此装置制备O2的化学方程式2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(4)用C装置收集氧气的依据是氧气不与空气成分反应,密度大于空气,检验收集到的气体是氧气的方法带火星的小木条放在集气瓶内,复燃说明是氧气.
分析 (1)根据实验室常用仪器解答;
(2)根据在加入药品之前应对实验装置进行的是:检查装置的气密性解答;
(3)根据制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热解答;
(4)根据氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.氧气的验满方法是:将带火星的木条平放在集气瓶内,木条复燃,证明是氧气解答.
解答 解:(1)根据实验室常用仪器可知:a酒精灯;b长颈漏斗;
(2)为确保制取气体的实验成功,在加入药品前应对装置进行气密性检查,防止因装置漏气而不能收集到气体且造成药品的浪费;
(3)实验室可利用加热分解高锰酸钾生成锰酸钾、二氧化锰、氧气的方法制取氧气,此时的发生装置应选A装置;也可使用过氧化氢在二氧化锰催化下分解生成水和氧气的反应制取,此时的发生装置应选B装置;而氧气密度大于空气、不易溶于水,因此收集氧气时可选择向上排空气法C装置进行收集,也可选择排水法E装置进行收集;反应的方程式为:2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑(或2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑);
(4)氧气不与空气成分反应,密度大于空气,可以向上排空气法C装置进行收集;氧气有助燃的作用,我们可以将带火星的小木条放在集气瓶内,复燃说明是氧气.
答案:
(1)a酒精灯;b长颈漏斗;
(2)检查装置的气密性;
(3)BC或BE;2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(4)氧气不与空气成分反应,密度大于空气,带火星的小木条放在集气瓶内,复燃说明是氧气.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了文字表达式的书写,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案(1)请写出稀硫酸与氢氧化钠反应的化学方程式:2NaOH+H2SO4=Na2SO4+2H2O;
(2)实验完成之后剩余溶液中的溶质一定有:NaOH、Na2SO4(写两种,填化学式,下同);
(3)为了进一步探究在滴加过程中为什么有气泡产生,下课后,小强决定继续探究,他首先提出了猜想:猜想一:稀硫酸中有杂质能和氢氧化钠溶液反应生成气体.
猜想二:氢氧化钠溶液中有杂质能和稀硫酸反应生成气体.
小强通过查阅资料获悉,遇到碱能够产生气体的物质一般都含有NH4+,遇到酸能够产生气体的物质一般都含有C${{O}_{3}}^{2-}$(填离子符号).对此,小强设计了如下实验进行探究:
| 实验步骤 | 实验现象 | 结论 |
| 取少量该稀硫酸于试管中,滴加过量的 Ca(OH)2溶液,仔细观察现象. | 没有明显现象 | 猜想一不正确 |
| 取少量该氢氧化钠溶液于试管中,滴加少量氢氧化钙溶液. | 有白色沉淀生成 | 猜想二正确 |
(4)小强经过认真思考,认为适量的加入一种试剂可以将氢氧化钠溶液中的杂质除去,这种试剂是氢氧化钙溶液.
| A. | 氮气约占空气质量的78%,氧气约占空气质量的21% | |
| B. | 氧气和氮气共约占空气体积的99%,其余的1%主要是二氧化碳 | |
| C. | 在测定空气里氧气的含量时,反应所消耗掉的气体是氧气 | |
| D. | 空气只是人类和动植物生存不可缺少的物质,再没有其他的用途 |
| A. | 蜡烛在空气中燃烧生成二氧化碳和水 | |
| B. | 氢气在氧气中燃烧发出黄色的火焰 | |
| C. | 碳在氧气中燃烧发出白光 | |
| D. | 铁丝在氧气中燃烧生成四氧化三铁 |