题目内容
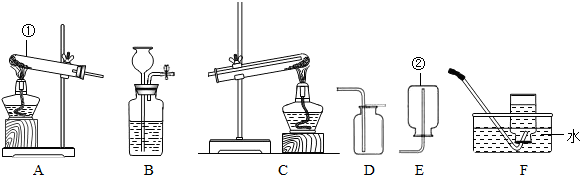
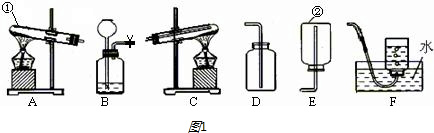
某同学用如图装置制氧气,请问: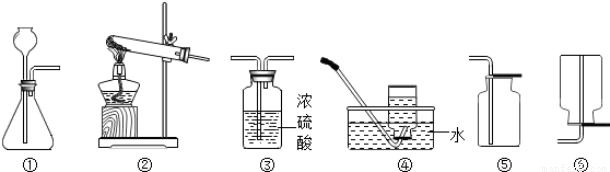
(1)用高锰酸钾制取和收集氧气的装置应选用 (填序号,下同);用双氧水和二氧化锰制取和收集干燥的氧气的装置应选用 .
(2)检查装置①气密性的方法是 .
(3)装置②试管口要略向下倾斜的原因是 .
(4)若用装置④收集的氧气不纯,其原因可能是(请写两种原因):
① ;
② .
【答案】分析:(1)用高锰酸钾制取氧气的发生装置属于固固加热型,收集氧气依据氧气的密度和溶解性选择;用双氧水和二氧化锰制取氧气的发生装置属于固液常温型,收集干燥的氧气要用浓硫酸干燥,且不能用排水法收集;
(2)检查该装置的气密性,应将两个口堵住一个,利用气压差来检验看长颈漏斗的液面变化,或用注射器推拉导气管,看长颈漏斗口的末端现象;
(3)试管口若向上倾斜会引起冷凝水倒流引起试管的炸裂;
(4)排水法一般收集的气体较纯,若不纯,可以从操作注意事项分析:①没有等到产生的气体均匀冒出,就开始收集 ②集气瓶的水没有装满,留有空气.
解答:解;(1)用高锰酸钾制取氧气的发生装置属于固固加热型,故选择发生装置是②,氧气不易溶于水、密度比空气大故可以采用排水法或向上排空气法收集,故可以是②④或②⑤;
用双氧水和二氧化锰制取氧气的发生装置属于固液常温型,故选择发生装置是①,收集干燥的氧气要用浓硫酸干燥,用向上排空气法收集不能用排水法收集,故需要③⑤;
故答案为:②④或②⑤;①③⑤;
(2)检查装置①气密性的原理是利用气压差,具体的操作步骤是:用止水夹夹住橡皮管,往长颈漏斗中加水,观察长颈漏斗能否形成高于锥形瓶液面的稳定水柱;
故答案为:用止水夹夹住橡皮管,往长颈漏斗中加水,观察长颈漏斗能否形成高于锥形瓶液面的稳定水柱;
(3)装置②试管口要略向下倾斜的原因是:防止冷凝水倒流到试管底部,造成试管炸裂;
故答案为:防止冷凝水倒流引起试管的炸裂;
(4)若用装置④排水法收集的氧气不纯,其可能的原因有:①没有等到产生的气体均匀冒出,就开始收集; ②集气瓶的水没有装满,留有空气;
故答案为:没等气泡连续均匀冒出时收集;集气瓶内没有装满水.
点评:本题主要考查了气体的制取装置和收集装置的选择以及实验的注意事项,气体的制取是初中重要的化学实验之一,既是重点,又是考查热点,要求学生在理解的基础上要熟练运用.
(2)检查该装置的气密性,应将两个口堵住一个,利用气压差来检验看长颈漏斗的液面变化,或用注射器推拉导气管,看长颈漏斗口的末端现象;
(3)试管口若向上倾斜会引起冷凝水倒流引起试管的炸裂;
(4)排水法一般收集的气体较纯,若不纯,可以从操作注意事项分析:①没有等到产生的气体均匀冒出,就开始收集 ②集气瓶的水没有装满,留有空气.
解答:解;(1)用高锰酸钾制取氧气的发生装置属于固固加热型,故选择发生装置是②,氧气不易溶于水、密度比空气大故可以采用排水法或向上排空气法收集,故可以是②④或②⑤;
用双氧水和二氧化锰制取氧气的发生装置属于固液常温型,故选择发生装置是①,收集干燥的氧气要用浓硫酸干燥,用向上排空气法收集不能用排水法收集,故需要③⑤;
故答案为:②④或②⑤;①③⑤;
(2)检查装置①气密性的原理是利用气压差,具体的操作步骤是:用止水夹夹住橡皮管,往长颈漏斗中加水,观察长颈漏斗能否形成高于锥形瓶液面的稳定水柱;
故答案为:用止水夹夹住橡皮管,往长颈漏斗中加水,观察长颈漏斗能否形成高于锥形瓶液面的稳定水柱;
(3)装置②试管口要略向下倾斜的原因是:防止冷凝水倒流到试管底部,造成试管炸裂;
故答案为:防止冷凝水倒流引起试管的炸裂;
(4)若用装置④排水法收集的氧气不纯,其可能的原因有:①没有等到产生的气体均匀冒出,就开始收集; ②集气瓶的水没有装满,留有空气;
故答案为:没等气泡连续均匀冒出时收集;集气瓶内没有装满水.
点评:本题主要考查了气体的制取装置和收集装置的选择以及实验的注意事项,气体的制取是初中重要的化学实验之一,既是重点,又是考查热点,要求学生在理解的基础上要熟练运用.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动.
提出问题 这种淡黄色粉末是什么?有什么性质和用途?
查阅资料 ①硫是淡黄色粉末,不溶于水;
②过氧化钠(Na2O2)是淡黄色粉末,溶于水并能与水反应,“载人宇宙飞船或潜水艇中一般都要安装盛放过氧化钠(Na2O2)颗粒的装置”
猜想与探究
猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物.
实验与结论
| 实验操作 | 实验现象 | 实验结论 | |
| 猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水,充分振荡 | ________ | 猜想a、c不成立,猜想b成立. |
提出猜想 过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气.
进行实验
实验Ⅰ:验证过氧化钠与氮气反应并生成氧气. 王轩同学设计如图Ⅰ所示装置:

(1)实验现象及结论:观察到________现象,判断过氧化钠与氮气没有发生反应.
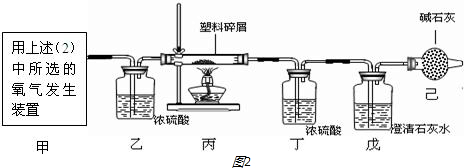
实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气. 华宇同学设计了如下图所示装置
(2)其中A装置的作用是________.
(3)实验现象及结论:带火星的木条复燃;查阅资料知道:过氧化钠与水蒸气生成了氧气和一种常见碱,写出该反应的化学方程式________.
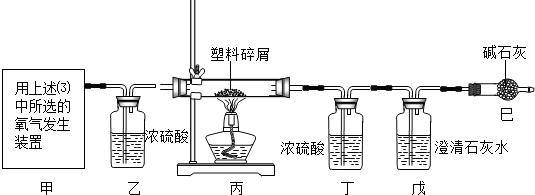
实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气.
李杰在老师的指导下也设计了如图Ⅱ所示装置.(不考虑稀盐酸的挥发)
(4)实验记录
| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 检查装置的气密性. 向装置中加入药品. | 装置的气密性良好. | |
| ② | 打开分液漏斗活塞,向A 装置中缓慢加入稀盐酸. | A装置中观察到的现象有________, C装置中有气泡出现. | A装置中发生反应的化学方程式为________; C装置作用是________. |
| ③ | 一段时间后用带火星的木条在D内进行检验. | 带火星的木条复燃. | 过氧化钠与二氧化碳反应并生成氧气. |
(1)张红同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是________.请你回答如何改进该实验________.
(2)王兵同学查阅资料后知道实验Ⅲ中过氧化钠与二氧化碳反应生成碳酸钠和氧气,他称取过氧化钠与二氧化碳充分反应后的固体剩余物质21.5g,加入到盛有足量稀盐酸的烧杯中,并不断用玻璃棒搅拌.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图Ⅳ所示(不考虑实验过程中其它因素的影响).
请计算碳酸钠的质量分数:________.(写出计算过程,结果保留一位小数)

某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动.
提出问题 这种淡黄色粉末是什么?有什么性质和用途?
查阅资料 ①硫是淡黄色粉末,不溶于水;
②过氧化钠(Na2O2)是淡黄色粉末,溶于水并能与水反应,“载人宇宙飞船或潜水艇中一般都要安装盛放过氧化钠(Na2O2)颗粒的装置”
猜想与探究
猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物.
实验与结论
提出问题 过氧化钠是否为一种制氧剂?与人呼出的哪种气体发生反应?
提出猜想 过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气.
进行实验
实验Ⅰ:验证过氧化钠与氮气反应并生成氧气. 王轩同学设计如图Ⅰ所示装置:
(1)实验现象及结论:观察到______现象,判断过氧化钠与氮气没有发生反应.
实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气. 华宇同学设计了如下图所示装置
(2)其中A装置的作用是______.
(3)实验现象及结论:带火星的木条复燃;查阅资料知道:过氧化钠与水蒸气生成了氧气和一种常见碱,写出该反应的化学方程式______.
实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气.
李杰在老师的指导下也设计了如图Ⅱ所示装置.(不考虑稀盐酸的挥发)
(4)实验记录
实验反思
(1)张红同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是______.请你回答如何改进该实验______.
(2)王兵同学查阅资料后知道实验Ⅲ中过氧化钠与二氧化碳反应生成碳酸钠和氧气,他称取过氧化钠与二氧化碳充分反应后的固体剩余物质21.5g,加入到盛有足量稀盐酸的烧杯中,并不断用玻璃棒搅拌.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图Ⅳ所示(不考虑实验过程中其它因素的影响).
请计算碳酸钠的质量分数:______.(写出计算过程,结果保留一位小数)
提出问题 这种淡黄色粉末是什么?有什么性质和用途?
查阅资料 ①硫是淡黄色粉末,不溶于水;
②过氧化钠(Na2O2)是淡黄色粉末,溶于水并能与水反应,“载人宇宙飞船或潜水艇中一般都要安装盛放过氧化钠(Na2O2)颗粒的装置”
猜想与探究
猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物.
实验与结论
| 实验操作 | 实验现象 | 实验结论 | |
| 猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水,充分振荡 | ______ | 猜想a、c不成立,猜想b成立. |
提出猜想 过氧化钠与人呼出的N2或CO2或水蒸气反应并生成氧气.
进行实验
实验Ⅰ:验证过氧化钠与氮气反应并生成氧气. 王轩同学设计如图Ⅰ所示装置:

(1)实验现象及结论:观察到______现象,判断过氧化钠与氮气没有发生反应.
实验Ⅱ:验证过氧化钠与水蒸气反应并生成氧气. 华宇同学设计了如下图所示装置
(2)其中A装置的作用是______.
(3)实验现象及结论:带火星的木条复燃;查阅资料知道:过氧化钠与水蒸气生成了氧气和一种常见碱,写出该反应的化学方程式______.
实验Ⅲ:验证过氧化钠与二氧化碳反应并生成氧气.
李杰在老师的指导下也设计了如图Ⅱ所示装置.(不考虑稀盐酸的挥发)
(4)实验记录
| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 检查装置的气密性. 向装置中加入药品. | 装置的气密性良好. | |
| ② | 打开分液漏斗活塞,向A 装置中缓慢加入稀盐酸. | A装置中观察到的现象有______, C装置中有气泡出现. | A装置中发生反应的化学方程式为______; C装置作用是______. |
| ③ | 一段时间后用带火星的木条在D内进行检验. | 带火星的木条复燃. | 过氧化钠与二氧化碳反应并生成氧气. |
(1)张红同学对实验Ⅲ的设计提出疑问:该实验不能证明二氧化碳与过氧化钠确实发生了反应,你认为他的理由是______.请你回答如何改进该实验______.
(2)王兵同学查阅资料后知道实验Ⅲ中过氧化钠与二氧化碳反应生成碳酸钠和氧气,他称取过氧化钠与二氧化碳充分反应后的固体剩余物质21.5g,加入到盛有足量稀盐酸的烧杯中,并不断用玻璃棒搅拌.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图Ⅳ所示(不考虑实验过程中其它因素的影响).
请计算碳酸钠的质量分数:______.(写出计算过程,结果保留一位小数)