题目内容
10.现有一包固体粉末,可能是碳酸钠、硫酸钠、硫酸铜、氯化钠,氢氧化钙中的-种或几种,为了测定其组成,取适量样品进行下列实验,请根据实验现象判断:(1)取样品溶于水,观察现象后,得出结论,原粉末中一定不含硫酸铜:能证明该结论的现象是得到无色澄清溶液.
(2)取上述溶液适量,加入足量的另一种物质后,观察现象,得出结论:原粉末中一定含有碳酸钠.由此可以推出,原溶液中一定不含有氢氧化钙.
(3)取步骤(1)试验后的溶液,加入X溶液后,再加入足量硝酸钡溶液,得到无色溶液A和白色沉淀B,取无色滤液A,加入Y溶液,得到无色溶液C.则
(1)加入Y溶液的目的是检验溶液中是否含有氯化钠.
(2)加入的X是硝酸,加入的量应该为过量(填“少量”、“适量”或“足量”)
(3)溶液C中含有的溶质是硝酸、硝酸钠、硝酸银、硝酸钡.
分析 根据硫酸铜在溶液中显蓝色,碳酸钠和氢氧化钙反应会生成碳酸钙沉淀和氢氧化钠,碳酸盐和酸反应会生成二氧化碳气体,氯离子和银离子反应会生成氯化银沉淀等知识进行分析.
解答 解:硫酸铜在溶液中显蓝色,碳酸钠和氢氧化钙反应会生成碳酸钙沉淀和氢氧化钠,碳酸盐和酸反应会生成二氧化碳气体,氯离子和银离子反应会生成氯化银沉淀,所以
(1)取样品溶于水,观察现象后,得出结论,原粉末中一定不含硫酸铜,能证明该结论的现象是:得到无色澄清溶液;
(2)取上述溶液适量,加入足量盐酸后,有气泡产生,得出结论:原粉末中一定含有碳酸钠,碳酸钠和氢氧化钙不能共存,由此可以推出,原溶液中一定不含有氢氧化钙;
(3)取步骤(1)试验后的溶液,加入硝酸溶液后,再加入足量硝酸钡溶液,得到无色溶液A和白色沉淀B,取无色滤液A,加入Y溶液,得到无色溶液C,则
加入Y溶液是硝酸银,目的是:检验溶液中是否含有氯化钠;
加入的X是硝酸,加入的量应该为过量;
通过推导可知,溶液C中含有的溶质是:硝酸、硝酸钠、硝酸银、硝酸钡.
故答案为:(1)得到无色澄清溶液;
(2)氢氧化钙;
(3)检验溶液中是否含有氯化钠;
硝酸,过量;
硝酸、硝酸钠、硝酸银、硝酸钡.
点评 在解此类题时,首先分析题中所给物质的性质,然后依据题中的现象确定各种物质的存在性,最后确定混合物的成分.

练习册系列答案
相关题目
18.2006年12月21日凌晨零时许,杭千高速杭州往千岛湖方向离建德乾潭不到2公里处,一辆装载危化品的车辆上掉落三大袋粉末状的化学物品.消防队员在处理该物品时,突然爆炸,两人脸部90%被炸伤.经多名专家鉴定,粉末是一种名叫氨基钠(NaNH2)的危险化学品,相对密度1.40、熔点210℃、沸点400℃,白色结晶性粉末易燃、易爆、有腐蚀性,与水接触后,会产生激烈的反应,生成氨和氢氧化钠.看到报道后,有人提出以下观点,你认为不正确的是( )
| A. | NaNH2与水接触后,能生成氨和氢氧化钠是它的化学性质 | |
| B. | NaNH2相对密度1.40、熔点210℃、沸点400℃是它的物理性质 | |
| C. | NaNH2在包装及贮运过程中,要求贮于阴凉干燥处,避免与空气、水、火接触 | |
| D. | 氨基钠有腐蚀性是因为其强碱性,其粉末易燃、易爆是因为其具有强的氧化性 |

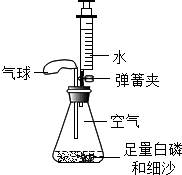 如图,锥形瓶内空气体积为230mL,注射器中水的体积为50mL,已知白磷的着火点40℃,该装置气密性良好.某实验小组利用如图所示装置测量空气中氧气体积分数并取得成功.在下列说法中:
如图,锥形瓶内空气体积为230mL,注射器中水的体积为50mL,已知白磷的着火点40℃,该装置气密性良好.某实验小组利用如图所示装置测量空气中氧气体积分数并取得成功.在下列说法中: