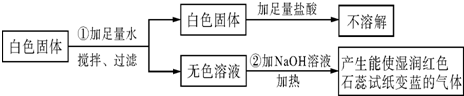
题目内容
13.如图为某学习小组探究金属化学性质时所做的四个实验,仔细分析后回答下列问题: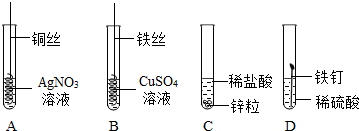
(1)描述A中的实验现象.铜丝表面附着了一层银白色物质,溶液由无色变成蓝色;
(2)写出C中反应的化学方程式Zn+2HCl═ZnCl2+H2↑.
分析 铜比银活泼,能和硝酸银反应生成硝酸铜和银,硝酸银溶液是无色的,硝酸铜溶液是蓝色的;
锌和稀盐酸反应生成氯化锌和氢气.
解答 解:(1)A中的实验现象是:铜丝表面附着了一层银白色物质,溶液由无色变成蓝色.
故填:铜丝表面附着了一层银白色物质,溶液由无色变成蓝色.
(2)锌和稀盐酸反应的化学方程式为:Zn+2HCl═ZnCl2+H2↑.
故填:Zn+2HCl═ZnCl2+H2↑.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
3.人体中化学元素含量的多少直接影响健康,缺乏下列哪种元素会引起骨质疏松( )
| A. | 碘 | B. | 钙 | C. | 锌 | D. | 铁 |
1.为探究皮蛋中的化学知识,同学们找来一包皮蛋加工配料,经过查找资料得知皮蛋加工配料的主要成分是氧化钙、纯碱和食盐.为了验证皮蛋加工配料的主要成分,他们进行了如下实验:
(1)取少量配料于小烧杯中,并向其中加入足量的水,搅拌、静置、过滤.过滤后得到的白色固体是碳酸钙.滤液中除了Na+之外,还一定存在氯离子和氢氧根 离子.
(2)若反应物没有恰好完全反应,滤液中还可能存在的离子是钙离子或碳酸根离子.为了进一步确定滤液中可能存在的离子,他们设计了如下实验,请你帮助他们完善:
你认为是否仍需进行实验进一步确认?否 (填“是”或“否”),理由是前一步实验已经判断出滤液中的成分了.
(1)取少量配料于小烧杯中,并向其中加入足量的水,搅拌、静置、过滤.过滤后得到的白色固体是碳酸钙.滤液中除了Na+之外,还一定存在氯离子和氢氧根 离子.
(2)若反应物没有恰好完全反应,滤液中还可能存在的离子是钙离子或碳酸根离子.为了进一步确定滤液中可能存在的离子,他们设计了如下实验,请你帮助他们完善:
| 实验步骤 | 实验现象 | 实验结论 |
| 取一只试管,倒入少量滤液,向其中滴加氢氧化钙溶液 | 若出现白色沉淀 | 说明滤液中含有碳酸根离子 |
| 若没有出现白色沉淀 | 说明滤液中含有钙离子 |
18.小王从新买的衣服边上取下一段线头在火上灼烧,闻到一股烧焦羽毛的气体,由此可判断这件衣服的面料是( )
| A. | 羊毛 | B. | 塑料 | C. | 棉麻织物 | D. | 麻 |
4.正确的实验操作对实验结果、人身安全都非常重要.在下图所示实验操作中正确的是( )
| A. |  闻气体气味 | B. |  移走蒸发皿 | C. |  倾倒液体 | D. |  稀释浓硫酸 |