题目内容
4.有一包固体粉末,可能是由含有CuSO4、Na2SO4、(NH4)2CO3、BaCl2、NH4Cl、KCl中的一种或几种组成的.为了分析固体粉末的成分,取少量该固体粉末进行实验,实验方案设计如下: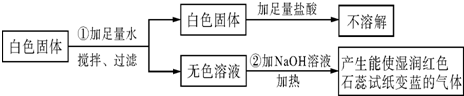
根据上述实验现象判断:
(1)白色固体中一定不含CuSO4、(NH4)2CO3,一定含有Na2SO4、BaCl2、NH4Cl.
(2)写出①中化学反应方程式:Na2SO4+BaCl2=BaSO4↓+2NaCl.
分析 根据题目给出的流程图和信息:由步骤①可知,白色固体中一定没有硫酸铜,因为硫酸铜溶于水呈蓝色;过滤得到的白色固体加入足量的盐酸不溶解,因此白色固体中一定有硫酸钡,原物质中一定有了氯化钡和硫酸钠,就一定不能再有碳酸铵了,因为碳酸钡溶于盐酸,此白色固体是硫酸钡,说明原混合物中一定有Na2SO4、BaCl2;由步骤②可知,加入氢氧化钠溶液加热,产生了能使湿润的红色石蕊试纸变蓝的气体,此气体是氨气,因此原白色固体中一定含有氯化铵;KCl可能有也可能没有.据此分析.
解答 解:(1)由步骤①可知,白色固体中一定没有硫酸铜,因为硫酸铜溶于水呈蓝色;过滤得到的白色固体加入足量的盐酸不溶解,因此白色固体中一定有硫酸钡,原物质中一定有了氯化钡和硫酸钠,就一定不能再有碳酸铵了,因为碳酸钡溶于盐酸,此白色固体是硫酸钡,说明原混合物中一定有Na2SO4、BaCl2;由步骤②可知,加入氢氧化钠溶液加热,产生了能使湿润的红色石蕊试纸变蓝的气体,此气体是氨气,因此原白色固体中一定含有氯化铵;KCl可能有也可能没有;
故答案为:CuSO4、(NH4)2CO3; Na2SO4、BaCl2、NH4Cl;
(2)①中是硫酸钠和氯化钡反应生成硫酸钡白色沉淀和氯化钠,配平即可,故其化学方程式为:Na2SO4+BaCl2=BaSO4↓+2NaCl.
点评 本题为框图式物质推断题,完成此题,关键是根据题干叙述,找准解题的突破口,直接得出有关物质的化学式,然后根据物质的性质结合框图得出其他物质的化学式.

练习册系列答案
相关题目
14.根据原子结构示意图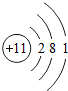 ,能够获得的信息是( )
,能够获得的信息是( )
①反应中得失电子数目 ②相对原子质量 ③原子的质子数 ④元素的化学性质.
 ,能够获得的信息是( )
,能够获得的信息是( )①反应中得失电子数目 ②相对原子质量 ③原子的质子数 ④元素的化学性质.
| A. | ②③ | B. | ①②④ | C. | ①③④ | D. | ②③④ |
15.生活中的变化属于化学变化的是( )
| A. | 冰融为水 | B. | 矿石粉碎 | C. | 食物腐败 | D. | 山体滑坡 |
12.最新发布的《环境空气质量标准》中增加了PM 2.5监测指标.PM 2.5是指大气中直径小于或等于2.5微米的颗粒物,是造成雾霾天气最主要的因素.下列做法不能有效遏制雾霾天气的是( )
| A. | 实施绿化工程,防治扬尘污染 | |
| B. | 加强对氢能源的开发、使氢气早日成为生活和生产中的主要燃料 | |
| C. | 为减少大气污染,火力发电厂应采取加高烟囱的办法 | |
| D. | 大力发展轻轨等公共交通,鼓励市民采用公交、自行车、步行等出行方式 |
19.如图为某反应的微观模拟示意图.从图中获得的有关信息不正确的是( )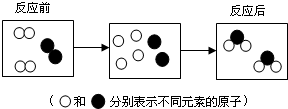

| A. | 原子是化学变化中的最小粒子 | |
| B. | 100个“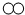 ”分子与50个“ ”分子与50个“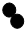 ”分子反应生成100个“ ”分子反应生成100个“ ”分子 ”分子 | |
| C. | 构成原子的微观粒子有质子、中子,电子 | |
| D. | 化学反应前后分子一定改变 |
16.小金同学在学习溶液知识后做了纠错整理,以下分析不合理的是( )
| A. | 60℃时50 g水中加入60g KNO3得105g饱和溶液则60℃时KNO3的溶解度是110g | |
| B. | 20℃时向20g饱和石灰水中加入少量生石灰,恢复到20℃时溶液中溶质的质量减小 | |
| C. | 硝酸钾的饱和溶液中含少量氯化钠时,可以通过冷却热饱和溶液的方法提纯硝酸钾 | |
| D. | 对固体溶质而言,温度不变时溶液从不饱和变成饱和,其质量分数不一定增大 |
 某实验室欲配制一定溶质质量分数的KNO3溶液,现实验室只含少量NaCl的KNO3固体药品.
某实验室欲配制一定溶质质量分数的KNO3溶液,现实验室只含少量NaCl的KNO3固体药品.