题目内容
在实验台上有三瓶未贴标签的溶液,已知分别是碳酸钠溶液、氢氧化钠溶液和稀盐酸。为区别这三种溶液,在老师指导下,兴趣小组的同学把这三种溶液按A、B、C进行编号,然后分别各取适量作为样品加入到三支试管中,进行了如右图所示的探究活动:
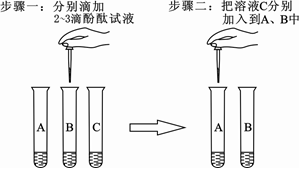
步骤一中,C无明显现象,A、B溶液的颜色变成红色,但A中红色马上褪去恢复为无色。
步骤二中,B溶液的颜色恰好由红色变成无色,且溶液中有气泡冒出;A溶液又变为红色。
下列关于此实验的叙述中正确的是
A. C溶液是氢氧化钠溶液
B. B溶液是稀盐酸
C. 步骤二中实验后B试管中溶质是氯化钠、酚酞
D. 步骤二中实验后A试管中溶质是氯化钠、酚酞

步骤一中,C无明显现象,A、B溶液的颜色变成红色,但A中红色马上褪去恢复为无色。
步骤二中,B溶液的颜色恰好由红色变成无色,且溶液中有气泡冒出;A溶液又变为红色。
下列关于此实验的叙述中正确的是
A. C溶液是氢氧化钠溶液
B. B溶液是稀盐酸
C. 步骤二中实验后B试管中溶质是氯化钠、酚酞
D. 步骤二中实验后A试管中溶质是氯化钠、酚酞
C
试题分析:这三种溶液中碳酸钠溶液和氢氧化钠溶液呈碱性,均能使酚酞变红;稀盐酸呈酸性,不能使酚酞变色,故C是稀盐酸;盐酸能与碳酸钠反应生成二氧化碳气体,由气泡产生,故B是碳酸钠溶液;由于酚酞只有在8.2~10.0时呈红色,故步骤二中溶液呈红色说明含有氢氧化钠和生成的氢氧化钠,D错误。故选C。

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目



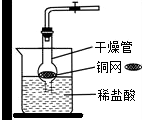
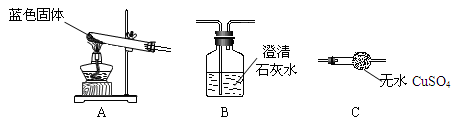
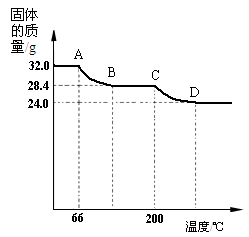


 三位同学利用电子天平共同作了以下测定实验,并记录如下实验数据。
三位同学利用电子天平共同作了以下测定实验,并记录如下实验数据。