题目内容
2.已知某固体粉末是由NaCl、Ba(NO3)2、CuSO4、Na2SO4、Na2CO3中的一种或几种组成,为了确定其成分,实验步骤如下:①取这种粉末加足量的水,振荡后呈浑浊,将该浑浊液分成二份;②向其中一份浑浊液中加入足量的稀盐酸,沉淀完全不溶解;③将另一份浑浊液过滤,得无色滤液,向该滤液中滴加AgNO3溶液,产生白色沉淀.请回答:(1)对原固体粉中一定不含有的物质是CuSO4和Na2CO3.
(2)步骤①中发生反应的化学方程式为Ba(NO3)2+Na2SO4=BaSO4↓+2NaNO3.
(3)判断原固体混合物中是否含有NaCl可能含有(填“含有/不含/可能含有”).
分析 钡离子能和硫酸根离子结合成白色沉淀硫酸钡,能和碳酸根离子结合成白色沉淀碳酸钡,硫酸钡不能和稀盐酸反应,碳酸钡能和稀盐酸反应生成氯化钡、水和二氧化碳;
硫酸铜溶液和硝酸铜溶液都是蓝色溶液;
硫酸根离子能和银离子结合成白色沉淀硫酸银,氯离子能和银离子结合成白色沉淀氯化银.
解答 解:钡离子能和硫酸根离子结合成白色沉淀硫酸钡,能和碳酸根离子结合成白色沉淀碳酸钡,硫酸钡不能和稀盐酸反应,碳酸钡能和稀盐酸反应生成氯化钡、水和二氧化碳;
硫酸铜溶液和硝酸铜溶液都是蓝色溶液;
硫酸根离子能和银离子结合成白色沉淀硫酸银,氯离子能和银离子结合成白色沉淀氯化银;
向其中一份浑浊液中加入足量的稀盐酸,沉淀完全不溶解,说明固体粉末中不含有碳酸钠,将另一份浑浊液过滤,得无色滤液,说明固体粉末中不含有硫酸铜,向该滤液中滴加AgNO3溶液,产生白色沉淀,白色沉淀可能是过量的硫酸钠和硝酸银反应生成的硫酸银,也可能是氯化钠和硝酸银反应生成的氯化银,也可能是过量的硫酸钠和硝酸银反应生成的硫酸银和氯化钠和硝酸银反应生成的氯化银,说明固体混合物中可能含有氯化钠,也可能不含有氯化钠;
(1)原固体粉中一定不含有的物质是CuSO4和Na2CO3;
(2)步骤①中,硝酸钡和硫酸钠反应生成硫酸钡沉淀和硝酸钠,发生反应的化学方程式为:Ba(NO3)2+Na2SO4=BaSO4↓+2NaNO3;
(3)原固体混合物中可能含有氯化钠,也可能不含有氯化钠.
故填:CuSO4和Na2CO3;Ba(NO3)2+Na2SO4=BaSO4↓+2NaNO3;可能含有.
点评 本题主要考查物质的性质,只有掌握了各种物质的性质,才能够判断物质之间相互转化时的反应物和生成物,从而可以进行各方面的判断.

练习册系列答案
相关题目
16.稀盐酸是化学实验中常用试剂,但下列试验中不宜使用稀盐酸的是( )
| A. | 除去氯化钙中的碳酸钙 | B. | 除去铜粉中的铁粉 | ||
| C. | 除去石灰石中的熟石灰 | D. | 除去铁丝中的铁锈 |
17.往AgNO3和Cu(NO3)2 的混合溶液中加入一定量的铁粉,充分反应后,过滤、洗涤,往滤渣中加入稀盐酸,有气泡冒出,则滤液中一定不存在的物质是( )
| A. | AgNO3、Cu(NO3)2、Fe (NO3 )2 | B. | Cu(NO3)2、Fe (NO3 )2 | ||
| C. | AgNO3、Cu(NO3)2 | D. | Fe (NO3 )2 |
10.我们知道物质有多种不同的分类方法,下列各组化合物中按某一条件,属于同一类的是( )
| A. | H2O、CaO、KClO3 | B. | KCl、KOH、KClO3 | ||
| C. | CO、CO2、H2CO3 | D. | CH4、聚乙烯塑料、顺丁橡胶 |
17.铁、铝、铜是常见的三种金属.同学们发现生活中的铝和铜制品表面一般不用防锈,而铁制品一般需要做防锈处理.
【提出问题】这是不是因为铁、铝、铜三种金属中铁的活动性最强呢?
【实验探究】同学们对这三种金属的活动性顺序展开了探究,请你参与探究并填写空格.
将粗细相同的铁丝、铝丝、铜丝分别插人体积相同、溶质质量分数也相同的稀盐酸中:
【讨论交流】为什么同一个实验得出了两种结论呢?同学们带着这个疑问查阅了相关资料,明白了铝丝在稀盐酸中短时间内无气泡,是因为铝表面致密的氧化膜会先与盐酸反应.
【反思评价】做金属性质实验时需将金属进行打磨,打磨的目的是除去金属表面的氧化物.
【实验验证】为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中:
写出铁与硫酸铜溶液反应的化学方程式Fe+CuSO4=FeSO4+Cu.
【拓展迁移】(1)若只有一支盛有少量稀盐酸的试管,只需合理安排金属丝的插人顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序.金属丝的插入顺序为铜铁铝或铁铜铝.
(2)金属被人类大规模开发利用的大致年限也与金属活动性顺序有关,请写出铁、铝、铜三种金属材料被人类利用的先后顺序Cu、Fe、Al.
【提出问题】这是不是因为铁、铝、铜三种金属中铁的活动性最强呢?
【实验探究】同学们对这三种金属的活动性顺序展开了探究,请你参与探究并填写空格.
将粗细相同的铁丝、铝丝、铜丝分别插人体积相同、溶质质量分数也相同的稀盐酸中:
| 操作 | 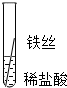 |  | 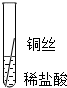 | 根据现象得出金属活动性顺序 |
| 片刻后现象 | 有少量气泡 | 无气泡 | 无气泡 | Fe>Al,Fe>Cu |
| 几分钟后现象 | 有少量气泡 | 有大量气泡 | 无气泡 |
【反思评价】做金属性质实验时需将金属进行打磨,打磨的目的是除去金属表面的氧化物.
【实验验证】为了进一步确认铁、铝、铜这三种金属的活动性顺序,同学们又将两根粗细相同的、打磨过的铁丝分别插入硫酸铝溶液、硫酸铜溶液中:
| 操作 |  | 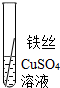 | 根据现象得出金属活动性顺序 |
| 现象 | 无明显现象 | 铁丝表面有红色物质析出 | Al>Fe>Cu |
【拓展迁移】(1)若只有一支盛有少量稀盐酸的试管,只需合理安排金属丝的插人顺序(能与盐酸反应的要一次将盐酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序.金属丝的插入顺序为铜铁铝或铁铜铝.
(2)金属被人类大规模开发利用的大致年限也与金属活动性顺序有关,请写出铁、铝、铜三种金属材料被人类利用的先后顺序Cu、Fe、Al.
11.下列物质之间,不存在如图所示转化关系的是(“→”表示能转化)( )
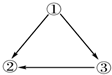

| A. | ①H2O2 ②H2O ③O2 | B. | ①Na2CO3 ②CO2 ③CaCO3 | ||
| C. | ①Ca(OH)2 ②CaCO3 ③NaOH | D. | ①O2 ②H2O ③CuO |
12.铝合金是工业中应用最广泛的一类有色金属结构材料,在航空、航天、汽车、机械制造、船舶及化学工业中已大量应用.工业经济的飞速发展,对铝合金的需求日益增多,使铝合金的研究也随之深入.已知某合金粉末除铝外,还含有铁、铜中的一种或两种.某兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究.
查阅资料:铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应.
猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有铜(填名称).
猜想3:该合金粉末中除铝外,还含有铁、铜.
实验探究:下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液.
探究结论:猜想3成立.
反思:一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.写出铝与稀盐酸反应的化学方程式2Al+6HCl═2AlCl3+3H2↑.
查阅资料:铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑( 产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应.
猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有铜(填名称).
猜想3:该合金粉末中除铝外,还含有铁、铜.
实验探究:下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液.
| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的30% NaOH溶液,充分反应后过滤,滤渣备用. | 粉末部分溶解,并有气体放出. | 合金中一定含有铝. |
| ②取步骤①所得滤渣,加过量的10% 盐酸,充分反应. | 滤渣部分溶解,并有气体放出,溶液呈浅绿色. | 合金中一定含有铁和铜. |
反思:一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.写出铝与稀盐酸反应的化学方程式2Al+6HCl═2AlCl3+3H2↑.