题目内容
2.某气体由N2、CO、N2O、SO2中的一种或几种组成,已知氧元素的质量分数为50%,则该气体的组成可能C
A.N2、N2O B.CO、SO2 C.N2、CO D.SO2.
分析 N2O、CO、SO2中的氧元素质量分数分别为:$\frac{16}{44}$×100%=36.4%,$\frac{16}{28}$×100%=57.1%,$\frac{32}{64}$×100%=50%.
解答 解:A、氮气中不含有氧元素,N2O中的氧元素质量分数是36.4%,因此氮气和一氧化二氮混合后,氧元素质量分数小于36.4%,该选项不符合题意;
B、CO、SO2中的氧元素质量分数分别为57.1%和50%,因此一氧化碳和二氧化硫混合后,氧元素质量分数大于50%,该选项不符合题意;
C、氮气中不含有氧元素,CO中的氧元素质量分数是57.1%,因此氮气和一氧化碳混合后,氧元素质量分数可能是50%,该选项符合题意;
D、二氧化硫中氧元素质量分数是50%,因此该气体可能是二氧化硫.
故选:C;
故填:SO2.
点评 本题主要考查元素质量分数的计算,计算时要注意准确性.

练习册系列答案
相关题目
13.如表知识归类正确的是( )
| 选项 | 归类 | 物质(或元素或微粒) |
| A | 可燃性气体 | 氢气、一氧化碳、氧气 |
| B | 常见合金 | 生铁、金刚石、武德合金 |
| C | 带电的微粒 | 原子核、电子、离子 |
| D | 氧化物 | 冰水、氨水、双氧水 |
| A. | A | B. | B | C. | C | D. | D |
10.对比是学习化学的重要方法.下列关于CO2和CO的各项对比,有错误的是( )
| 选项 | 共性 | 差异性 |
| A | 均有碳元素和氧元素组成 | 元素的质量比不同 |
| B | 均由分子构成 | 分子的种类不同 |
| C | 均能与水化合 | 化合时现象不同 |
| D | 常温下均是无色气体 | 相同条件下气体的密度不同 |
| A. | A | B. | B | C. | C | D. | D |
7.下列事实的解释正确的B
| 序号 | 事 实 | 解 释 |
| A | 氧气用于金属切割 | 氧气具有可燃性 |
| B | 石墨用来制取金刚石 | 石墨中的碳原子可以重新排列 |
| C | 墨汁写的字或作的画可永久保存 | 碳的化学性质在任何条件都不活泼 |
| D | 做铁丝燃烧实验时集气瓶底部预先要留少量水 | 防止高温熔落物溅落而炸裂集气瓶 |
12.有一种石灰石样品,某同学想测定该石灰石样品的纯度,他取用2克石灰石样品,把20克稀盐酸分成四次加入(杂质不反应,加热也不挥发不分解),充分反应后剩余固体的质量见下表所示:
(1)从表中分析,第三次加入稀盐酸反应结束.
(2)石灰石样品的纯度是80%.
(3)125千克这样的石灰石固体充分煅烧后,最终得到的固体质量是对少千克?
(1)从表中分析,第三次加入稀盐酸反应结束.
(2)石灰石样品的纯度是80%.
(3)125千克这样的石灰石固体充分煅烧后,最终得到的固体质量是对少千克?
| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入5g | 1.315g |
| 第二次加入5g | 0.63g |
| 第三次加入5g | 0.4g |
| 第四次加入5g | 0.4g |
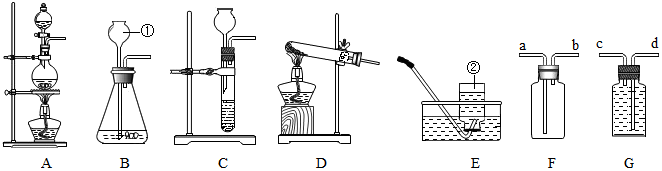

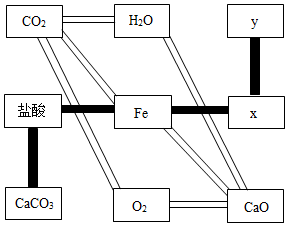 联欢会上,同学们设计了用于解锁屏幕的“化学键盘”,九个键分别代表不同的物质.如下图所示:
联欢会上,同学们设计了用于解锁屏幕的“化学键盘”,九个键分别代表不同的物质.如下图所示:
