题目内容
18.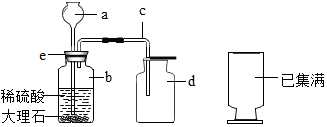 观察如图实验装置:
观察如图实验装置:(1)改正实验室制取二氧化碳中的错误
①不能用稀硫酸
②收集二氧化碳时导管要伸到集气瓶底部
③收集满二氧化碳的集气瓶要正放在桌面上
(2)写出实验仪器名称
a长颈漏斗;d集气瓶;
(3)如果把生成的气体通入石蕊试液中,石蕊液就变成红色,把颜色变化了的液体加热,又恢复原来的紫色;检验二氧化碳气体就是把气体通入到澄清的石灰水中;该反应的方程式是CO2+Ca(OH)2=CaCO3↓+H2O.
分析 (1)根据实验室二氧化碳正确的装置,收集进行分析解答本题;
(2)熟记仪器的名称;
(3)根据二氧化碳和水反应生成碳酸及碳酸不稳定受热易分解以及化学方程式的写法来分析.
解答 解:(1)用稀盐酸,不能用稀硫酸,收集二氧化碳时导管要伸到集气瓶底部,收集满二氧化碳的集气瓶要正放在桌面上,故填:①不能用稀硫酸;②收集二氧化碳时导管要伸到集气瓶底部;③收集满二氧化碳的集气瓶要正放在桌面上;
(2)a是长颈漏斗,d是集气瓶;故填:长颈漏斗;集气瓶;
(3)二氧化碳和水反应生成碳酸显酸性,能使紫色的石蕊试液变成红色,反应的方程式为:H2O+CO2=H2CO3;而碳酸不稳定,受热易分解为二氧化碳和水,酸性消失,故红色又变成紫色,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水;故填:红;紫;CO2+Ca(OH)2=CaCO3↓+H2O.
点评 给实验装置指错误要按一定的顺序去观察装置,找错误,否则容易遗漏.通常按从下到上,从左到右,从发生装置到收集装置.同时还要考虑制取不同的气体装置的特点,这样综合分析,就能将错误找全、找准.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.长久使用的热水瓶底部有一层水垢.为了除去热水瓶底部的水垢,研究性学习小组的同学进行了下列研究和实验:
【查阅资料】水垢的主要成分是CaCO3和Mg(OH)2.
【实验】取50g水垢的样品(杂质不与盐酸和水反应)放入烧杯中,加入足量的质量分数为10%盐酸,使样品完全反应,并记录反应过程中混合物质量的变化.烧杯及样品和稀盐酸的质量(m)起始时为300g.实验数据记录如表:
【分析与研究】
(1)分析表中记录的数据,你认为反应时间为8min时记录的质量数据是错误的.
(2)Mg(OH)2中镁、氧、氢三种元素的质量比为12:16:1.Mg(OH)2与盐酸反应化学方程式为Mg(OH)2+2HCl=MgCl2+2H2O.
(3)反应后的混合物中含有CaCl2和MgCl2.9.5g MgCl2含有的氯元素的质量与7.3g HCl含有的氯元素的质量相当.
(4)水垢中碳酸钙的质量分数是多少?(请保留计算过程)
【查阅资料】水垢的主要成分是CaCO3和Mg(OH)2.
【实验】取50g水垢的样品(杂质不与盐酸和水反应)放入烧杯中,加入足量的质量分数为10%盐酸,使样品完全反应,并记录反应过程中混合物质量的变化.烧杯及样品和稀盐酸的质量(m)起始时为300g.实验数据记录如表:
| 反应时间(min) | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 |
| m(g) | 294.5 | 290.0 | 286.0 | 286.0 | 283.0 | 282.4 | 282.4 | 282.4 |
(1)分析表中记录的数据,你认为反应时间为8min时记录的质量数据是错误的.
(2)Mg(OH)2中镁、氧、氢三种元素的质量比为12:16:1.Mg(OH)2与盐酸反应化学方程式为Mg(OH)2+2HCl=MgCl2+2H2O.
(3)反应后的混合物中含有CaCl2和MgCl2.9.5g MgCl2含有的氯元素的质量与7.3g HCl含有的氯元素的质量相当.
(4)水垢中碳酸钙的质量分数是多少?(请保留计算过程)
13.ag硫在bg氧气中恰好完全燃烧,生成cg二氧化硫,下列叙述不正确的是( )
| A. | a与b之和等于c | |
| B. | 反应前后硫原子总数、氧原子总数不变 | |
| C. | 反应前后各元素的化合价不变 | |
| D. | 反应前后硫元素和氧元素种类不变 |
3.一氧化碳和二氧化碳的相同点是( )
| A. | 利于动植物生长 | B. | 都能还原氧化铜 | ||
| C. | 都能燃烧 | D. | 都是无色的氧化物 |

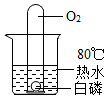 水是人类宝贵的自然资源.
水是人类宝贵的自然资源.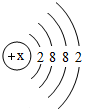 :
:
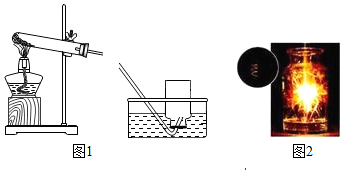 绘制实验设计图是填写实验报告常用的一项重要技能.如图是某同学正在绘制的实验室用高锰酸钾制取氧气的装置图.
绘制实验设计图是填写实验报告常用的一项重要技能.如图是某同学正在绘制的实验室用高锰酸钾制取氧气的装置图.