题目内容
13.ag硫在bg氧气中恰好完全燃烧,生成cg二氧化硫,下列叙述不正确的是( )| A. | a与b之和等于c | |
| B. | 反应前后硫原子总数、氧原子总数不变 | |
| C. | 反应前后各元素的化合价不变 | |
| D. | 反应前后硫元素和氧元素种类不变 |
分析 A、依据质量守恒定律可知参加反应的各物质质量之和等于生成物的质量总和.
B、依据质量守恒定律分析,反应前后各原子种类不变.
C、根据单质中元素化合价为零分析.
D、依据质量守恒定律分析,反应前后元素种类不变.
解答 解:A、ag硫在bg氧气中恰好完全燃烧,生成cg二氧化硫,依据质量守恒定律a+b=c,故A说法正确;
B、依据质量守恒定律,反应前后各原子种类不变,因此反应前后硫、氧原子总数都不变,故B说法正确;
C、单质中元素化合价为零,化合物中不为零,化合价发生了改变,故C说法错误;
D、依据质量守恒定律,反应前后元素种类不变,所以反应前后硫元素和氧元素的种类不变,故D说法正确.
故选C.
点评 此题是对质量守恒定律的考查,解题的关键是理解质量守恒定律的内容和微观解释,属基础性知识考查题.

练习册系列答案
相关题目
4.地壳中含量最多的金属元素是( )
| A. | 铝 | B. | 铁 | C. | 氧 | D. | 硅 |
8. 已知:Ca(HCO3)2 $\frac{\underline{\;\;△\;\;}}{\;}$ CaCO3+CO2↑+H2O.如图表示一定质量的Ca(HCO3)2受热过程中某变量y随时间的变化趋势(该过程中CaCO3不分解),则y表示的是( )
已知:Ca(HCO3)2 $\frac{\underline{\;\;△\;\;}}{\;}$ CaCO3+CO2↑+H2O.如图表示一定质量的Ca(HCO3)2受热过程中某变量y随时间的变化趋势(该过程中CaCO3不分解),则y表示的是( )
 已知:Ca(HCO3)2 $\frac{\underline{\;\;△\;\;}}{\;}$ CaCO3+CO2↑+H2O.如图表示一定质量的Ca(HCO3)2受热过程中某变量y随时间的变化趋势(该过程中CaCO3不分解),则y表示的是( )
已知:Ca(HCO3)2 $\frac{\underline{\;\;△\;\;}}{\;}$ CaCO3+CO2↑+H2O.如图表示一定质量的Ca(HCO3)2受热过程中某变量y随时间的变化趋势(该过程中CaCO3不分解),则y表示的是( )| A. | Ca(HCO3)2的质量 | B. | 固体中氧元素的质量 | ||
| C. | 固体中钙元素的质量 | D. | 固体中钙元素的质量分数 |
5.在一个密闭容器中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表:
下列说法中,不正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 18 | 1 | 2 | 32 |
| 反应后质量/g | X(未知) | 26 | 2 | 12 |
| A. | 乙是反应物 | B. | 反应中乙、丁的质量比为 5:4 | ||
| C. | 反应后物质甲的质量为 13g | D. | 物质丙可能是该反应的催化剂 |
2.下列有关实验现象描述正确的是( )
| A. | 红磷在空气中燃烧,放出热量,产生大量白色烟雾 | |
| B. | 铁丝在空气中剧烈燃烧,火星四射,生成黑色固体 | |
| C. | 木炭在氧气中燃烧,发出白光,产生二氧化碳气体 | |
| D. | 硫粉在氧气中燃烧,发出明亮的蓝紫色火焰 |
4. 全球近140个国家将根据签署的《国际防治汞污染公约》,在2020年前禁止生产和进出口含汞产品,如电池、荧光灯、化妆品、温度计、血压计等.分析如图判断关于汞元素的相关信息正确的是( )
全球近140个国家将根据签署的《国际防治汞污染公约》,在2020年前禁止生产和进出口含汞产品,如电池、荧光灯、化妆品、温度计、血压计等.分析如图判断关于汞元素的相关信息正确的是( )
 全球近140个国家将根据签署的《国际防治汞污染公约》,在2020年前禁止生产和进出口含汞产品,如电池、荧光灯、化妆品、温度计、血压计等.分析如图判断关于汞元素的相关信息正确的是( )
全球近140个国家将根据签署的《国际防治汞污染公约》,在2020年前禁止生产和进出口含汞产品,如电池、荧光灯、化妆品、温度计、血压计等.分析如图判断关于汞元素的相关信息正确的是( )| A. | 汞为非金属元素 | B. | 汞原子的质量为200.6g | ||
| C. | 汞原子的中子数是80 | D. | 汞的化学式为Hg |
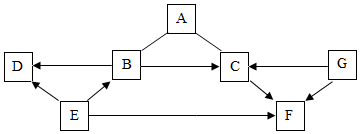 图中A~G是初中化学常见的物质,且分别是由O、C、Al、Fe、Cu中的一种或两种元素组成的.在通常情况下,A、B、D与其他物质的状态不同,其中D、B为化合物,D中两种元素质量之比为3:8;E固体具有疏松多孔的结构,可用来净化水;F为紫红色固体,G在空气中表面生成一层致密的氧化膜,具有很好的抗腐蚀性能.图中“--”表示两端的物质间能够发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去.
图中A~G是初中化学常见的物质,且分别是由O、C、Al、Fe、Cu中的一种或两种元素组成的.在通常情况下,A、B、D与其他物质的状态不同,其中D、B为化合物,D中两种元素质量之比为3:8;E固体具有疏松多孔的结构,可用来净化水;F为紫红色固体,G在空气中表面生成一层致密的氧化膜,具有很好的抗腐蚀性能.图中“--”表示两端的物质间能够发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去.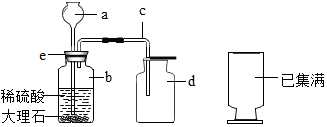 观察如图实验装置:
观察如图实验装置: