题目内容
15.(1)2017年,我省将有多条高铁开通,人们的出行将更加方便、快捷.结合所学化学知识,回答下列问题:①动车电路中导线大多是用铜制的,这是利用了铜的延展性和导电性.动车使用的金属材料大多是合金而不是纯金属,这是因为合金具有更多优良性能,例如,钢比纯铁硬度大(填“大”或“小”);
②动车表面喷漆除美观外,主要是为了防止外壳生锈,其防锈的原理是隔绝氧气和水;铁在潮湿的空气中就会生锈,铁锈可用稀盐酸除去,该反应的化学方程式是Fe2O3+6HCl═2FeCl3+3H2O.铁和氧气在点燃条件下能发生反应,其反应的现象是剧烈燃烧、火星四射、生成黑色固体.
(2)已知M、N、R三种金属存在如下反应:R+NCl2═N+RCl2;M+RCl2═R+MCl2,这两个反应的基本反应类型都是置换反应,M、N、R三种金属的活动性由强到弱的顺序为M>R>N.
分析 (1)根据金属的物理性质以及合金的特点来分析;
根据防锈的原理、化学反应的原理以及现象来分析;
(2)根据化学反应类型的特点以及金属的活动性来分析.
解答 解:(1)①动车电路中导线大多是用铜制的,这是利用了铜的延展性和导电性;合金的硬度比组成金属的硬度大,所以钢比纯铁硬度大;故填:导电性;大;
②铁在空气中锈蚀,实际上是铁跟空气中的氧气和水共同作用的结果,动车表面喷漆主要是为了防止外壳生锈,其原理是隔绝水和氧气(或空气);
铁锈的主要成分是氧化铁,氧化铁能与盐酸反应生成氯化铁和水,细铁丝在氧气中剧烈燃烧、火星四射、生成黑色固体;故填:隔绝氧气和水;Fe2O3+6HCl═2FeCl3+3H2O;剧烈燃烧、火星四射、生成黑色固体;
(2)这两个反应都是由单质与化合物反应生成新的单质与新的化合物,属于置换反应;由金属的活动性可知,排在前面的金属可以将排在后面的金属从其盐溶液中置换出来,故填:置换反应;M>R>N.
点评 本题考查的是金属的有关性质,完成此题,可以依据已有的知识结合金属活动性顺序的知识进行.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
6.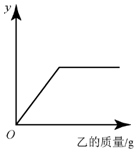 向下表中的乙物质中逐渐加入一定质量的甲物质至过量,其相关量y与所加乙物质的质量关系与如图不相符的是( )
向下表中的乙物质中逐渐加入一定质量的甲物质至过量,其相关量y与所加乙物质的质量关系与如图不相符的是( )
 向下表中的乙物质中逐渐加入一定质量的甲物质至过量,其相关量y与所加乙物质的质量关系与如图不相符的是( )
向下表中的乙物质中逐渐加入一定质量的甲物质至过量,其相关量y与所加乙物质的质量关系与如图不相符的是( )| 选项 | 甲 | 乙 | y |
| A | Zn | 稀硫酸 | 生成气体的质量 |
| B | NaOH溶液 | FeCl3溶液 | 混合后溶液的质量 |
| C | Al2O3 | 稀盐酸 | 生成水的质量 |
| D | CaCl2溶液 | Na2CO3 | 生成沉淀的质量 |
| A. | A | B. | B | C. | C | D. | D |
3.实验操作的规范和准确直接影响实验的成功和安全,以下实验操作中,正确的是( )
| A. |  稀释浓硫酸 | B. |  干燥CO2 | C. |  蒸发溶剂结晶 | D. |  收集甲烷 |
7.氯化镁是制取镁的原料之一,现要测定某化工产品(含MgCl2和KCl)中所含的氯化镁质量分数,进行实验:先将10g样品完全溶于水,然后把50g一定质量分数的氢氧化钾溶液平均分五次加入样品溶液中,充分振荡,实验所得数据如表:
请分析上述数据,回答下列问题
(1)表中a为1.16.
(2)样品中的氯化钾属于化肥中的钾肥,可回收利用.
(3)计算样品中氯化镁的质量分数是多少?(写出计算过程)
| 编号 | 1 | 2 | 3 | 4 | 5 |
| 加入氢氧化钾溶液的质量/g | 10 | 10 | 10 | 10 | 10 |
| 生成沉淀的质量/g | 0.58 | a | 1.74 | 2.32 | 2.32 |
(1)表中a为1.16.
(2)样品中的氯化钾属于化肥中的钾肥,可回收利用.
(3)计算样品中氯化镁的质量分数是多少?(写出计算过程)
4.下列4个图象能正确反映对应的实验操作的是( )
| A. | 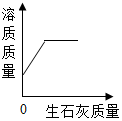 向一定量的饱和Ca(OH)2溶液中加入一定量的生石灰 | |
| B. | 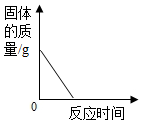 向一定量的CuO中通入CO气体并加热 | |
| C. | 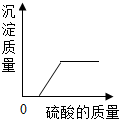 向一定量的KOH和Ba(NO3)2的混合溶液中,逐滴加入稀H2SO4 | |
| D. | 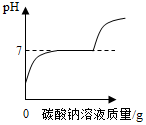 向一定量的HCl和CaCl2(CaCl2溶液呈中性)的混合液中加入Na2CO3溶液 |
5. 如图所示,广口瓶中盛有气体X,胶头滴管中盛有液体Y.若挤压胶头滴管使液体滴入瓶中振荡,一段时间后可见小气球a膨胀鼓起.下列各组物质不会出现上述现象的是( )
如图所示,广口瓶中盛有气体X,胶头滴管中盛有液体Y.若挤压胶头滴管使液体滴入瓶中振荡,一段时间后可见小气球a膨胀鼓起.下列各组物质不会出现上述现象的是( )
 如图所示,广口瓶中盛有气体X,胶头滴管中盛有液体Y.若挤压胶头滴管使液体滴入瓶中振荡,一段时间后可见小气球a膨胀鼓起.下列各组物质不会出现上述现象的是( )
如图所示,广口瓶中盛有气体X,胶头滴管中盛有液体Y.若挤压胶头滴管使液体滴入瓶中振荡,一段时间后可见小气球a膨胀鼓起.下列各组物质不会出现上述现象的是( )| X | Y | |
| A | CO2 | Ca(OH)2 |
| B | CO | NaOH |
| C | HCl | Ca(OH)2 |
| D | SO2 | NaOH |
| A. | A | B. | B | C. | C | D. | D |
