题目内容
15.下列现象的解释或结论正确的是( )| A. | 把活性炭投入到红墨水中墨水红色褪去--发生了化学变化 | |
| B. | 气体受热膨胀--气体分子受热体积变大 | |
| C. | 把燃烧着的木条伸入集气瓶中木条熄灭--瓶中气体一定是二氧化碳 | |
| D. | 用嘴吹灭燃烧着的蜡烛--降低蜡烛的温度 |
分析 A、根据化学变化的概念进行分析;B、根据物质受热膨胀的原因考虑;C、根据常见气体的性质考虑;D、根据灭火的原理考虑.
解答 解:A、把活性炭投入到红墨水中墨水红色褪去发生了物理变化,故错;
B、物质受热膨胀是由于升高温度,分子运动速度加快,分子之间间隔变大,分子的体积大小没变,故B错;
C、把燃着的木条伸入集气瓶中,木条熄灭,瓶中气体不一定是CO2,氮气也不支持燃烧,故C错;
D、用嘴吹灭燃烧着的蜡烛是降低蜡烛的温度到着火点以下,故D正确.
故选D.
点评 本题难度不大,综合性比较强,涉及了多个知识点,灵活运用分子的性质、灭火的原理以及常见气体的性质等是顺利解题的关键.

练习册系列答案
相关题目
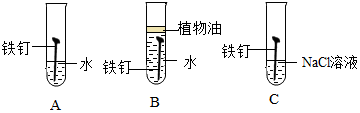
6.如是同学们运甩对比的方法探究碱的性质.
(1)由实验一、二可知,氢氧化钠会吸收空气中的二氧化碳和水,因此要密封保存.
(2)实验三中可观察到三个软塑料瓶变瘪的程度大小为A>B>C,A瓶中发生反应的化学方程式为CO2+2NaOH=Na2CO3+H2O,对比A瓶与C(选填“B”或“C”)瓶的实验现象,可证明CO2能与NaOH发生反应.
| 实验一 | 实验二 | 实验三 |
 |  |  |
(2)实验三中可观察到三个软塑料瓶变瘪的程度大小为A>B>C,A瓶中发生反应的化学方程式为CO2+2NaOH=Na2CO3+H2O,对比A瓶与C(选填“B”或“C”)瓶的实验现象,可证明CO2能与NaOH发生反应.
4.下列现象属于化学变化的是( )
| A. | 瓷碗破碎 | B. | 干冰升华 | C. | 铁锅生锈 | D. | 制合金 |
5.分类是学习化学的常用方法,下列物质的归类完全正确的是( )
| A. | 具有可燃性气体:氢气、一氧化碳、二氧化碳 | |
| B. | 氧化物:SO2、KClO3、H2O | |
| C. | 合金:生铁、不锈钢、黄铜 | |
| D. | 化石燃料:石油、煤、木材 |
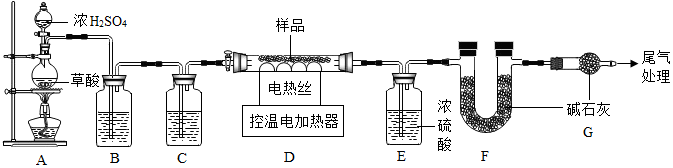
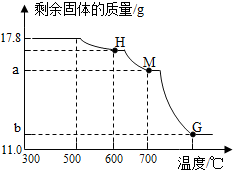
 构建知识网络是一种重要的学习方法,如图是关于E物质的知识网络,E物质是海洋中最多的一种物质,C物质的组成元素与E完全相同,D物质存在于汽水中,B物质是一种单质,具有助燃性;A物质组成元素中含有金属元素(注意:反应条件、部分反应物和生成物没有给出).
构建知识网络是一种重要的学习方法,如图是关于E物质的知识网络,E物质是海洋中最多的一种物质,C物质的组成元素与E完全相同,D物质存在于汽水中,B物质是一种单质,具有助燃性;A物质组成元素中含有金属元素(注意:反应条件、部分反应物和生成物没有给出).