题目内容
3.属于溶液的是( )| A. | 石灰乳 | B. | 牛奶 | C. | 矿泉水 | D. | 蓝莓果酱 |
分析 溶液是均一、稳定的混合物;溶液的本质特征是均一性、稳定性,属于混合物;据此分析判断.
解答 解:A、石灰乳是氢氧化钙固体悬浮于水中形成的,是不均一、不稳定的混合物,属于悬浊液,不属于溶液,故选项错误.
B、牛奶是不溶性的小液滴等分散到液体中形成的,不均一、不稳定,不属于溶液,故选项错误.
C、矿泉水是矿物质溶于水形成的,是均一、稳定的混合物,属于溶液,故选项正确.
D、蓝莓果酱不属于溶液,故选项错误.
故选C
点评 本题难度不大,掌握溶液的本质特征(均一性、稳定性、混合物)是解答本题的关键.

练习册系列答案
相关题目
9.根据某燃料X完全燃烧的化学方程式:X+3O2$\stackrel{点燃}{→}$2CO2+3H2O,判断错误的是( )
| A. | X的化学式为C2H6O | |
| B. | X是有机物 | |
| C. | 化学方程式中各物质的系数比与物质的量之比相等 | |
| D. | 该反应前后分子的个数没有发生改变 |
14.下列有关元素的叙述正确的是( )
| A. | 质子数相同的两种粒子一定属于同种元素 | |
| B. | 同种元素的原子结构和质量完全相同 | |
| C. | 元素的种类是由核内质子数决定的 | |
| D. | 元素是具有相同中子数的一类原子的总称 |
8.属于同素异形体的是( )
| A. | 金刚石和C60 | B. | 氧气和液氧 | C. | 蒸馏水和矿泉水 | D. | 干冰和冰 |
15.如表是KNO3、NaCl在不同温度下的部分溶解度数据,请回答问题:
①10℃时,NaCl溶解度是35.8g.
②在20℃时,将50克硝酸钾溶解在100克水中,形成的是饱和(填“饱和”或“不饱和”)溶液,若升温至40℃,形成的溶液质量为150g,则烧杯中溶液的溶质质量分数为33.3%(精确到0.1%)
③某温度时,氯化钠与硝酸钾的溶解度相等,则溶解度的最小取值范围是36g<S<36.6g.
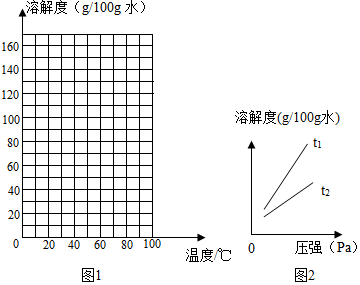
④根据表中数据,请在图1坐标图中描点、绘制符合KNO3溶解度变化规律的曲线如图.
⑤固体硝酸钾中混有少量氯化钠可以通过溶解、蒸发浓缩、降温结晶、过滤等步骤分离提纯硝酸钾.可以利
用该方法分离的理由是ⅠⅡ.
Ⅰ.固体混合物中硝酸钾的含量较高,氯化钠的含量较低
Ⅱ.硝酸钾的溶解度受温度影响变化较大
Ⅲ.40℃至100℃,硝酸钾的溶解度始终大于氯化钠
⑥气体的溶解度也有一定的变化规律.
不同温度下,氧气的溶解度随压强变化如图2所示,图中t2对应的温度为30℃,则t1对应的温度A.
A.小于30℃B.等于30℃C.大于30℃D.无法确定.
| 温度(℃) | 10 | 20 | 40 | 60 | 80 |
| KNO3 | 20.9 | 31.6 | 63.9 | 110 | 169 |
| NaCl | 35.8 | 36 | 36.6 | 37.3 | 38.4 |
②在20℃时,将50克硝酸钾溶解在100克水中,形成的是饱和(填“饱和”或“不饱和”)溶液,若升温至40℃,形成的溶液质量为150g,则烧杯中溶液的溶质质量分数为33.3%(精确到0.1%)
③某温度时,氯化钠与硝酸钾的溶解度相等,则溶解度的最小取值范围是36g<S<36.6g.
④根据表中数据,请在图1坐标图中描点、绘制符合KNO3溶解度变化规律的曲线如图.

⑤固体硝酸钾中混有少量氯化钠可以通过溶解、蒸发浓缩、降温结晶、过滤等步骤分离提纯硝酸钾.可以利
用该方法分离的理由是ⅠⅡ.
Ⅰ.固体混合物中硝酸钾的含量较高,氯化钠的含量较低
Ⅱ.硝酸钾的溶解度受温度影响变化较大
Ⅲ.40℃至100℃,硝酸钾的溶解度始终大于氯化钠
⑥气体的溶解度也有一定的变化规律.
不同温度下,氧气的溶解度随压强变化如图2所示,图中t2对应的温度为30℃,则t1对应的温度A.
A.小于30℃B.等于30℃C.大于30℃D.无法确定.
12.糖水属于( )
| A. | 悬浊液 | B. | 乳浊液 | C. | 溶液 | D. | 纯净物 |
13.某小组同学设计并进行实验,探究影响过氧化氢分解速率的因素.(实验装置如图1所示,夹持仪器已略去)
【猜想与假设】影响过氧化氢分解速率的因素可能有温度、
溶液的浓度、催化剂种类.
【实验记录】同学们进行6组实验,实验记录如表:
【解释与结论】
(1)实验②中应加入过氧化氢溶液的体积x是6mL.
(2)实验①~⑥通过测定相同时间内产生氧气的体积来比较过氧化氢的分解速率,还可以通过测定产生相同体积的氧气所需的时间来比较过氧化氢的分解速率.
(3)得出“过氧化氢溶液的浓度越大分解速率越大”结论所依据的实验是③④(填序号).
(4)通过实验①、②、④可得出的结论是温度越高,过氧化氢分解速率越大.
【反思与评价】
(5)同学们认为实验室制氧气,应选择实验⑥而不选实验②的理由是相同时间内实验②产生氧气少;需要加热;水蒸气含量高(答两点).
(6)某同学改用如图2所示装置代替气囊完成实验②,正确的实验操作顺序是a.
a.将导管伸入量筒,开启控温加热器,滴入过氧化氢溶液
b.开启控温加热器,将导管伸入量筒,滴入过氧化氢溶液
c.开启控温加热器,滴入过氧化氢溶液,待导管口有连续均匀气泡冒出时将导管伸入量筒.

【猜想与假设】影响过氧化氢分解速率的因素可能有温度、
溶液的浓度、催化剂种类.
【实验记录】同学们进行6组实验,实验记录如表:
| 实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 过氧化氢溶液的浓度(%) | 30 | 30 | 15 | 30 | 30 | 30 |
| 过氧化氢溶液的体积(mL) | 6 | x | 6 | 6 | 6 | 6 |
| 水槽中水的温度 | 20 | 90 | 70 | 70 | 20 | 20 |
| 锥形瓶中的物质 | ----- | ----- | ----- | ----- | 0.5gNaCl | 0.5gFeCl3 |
| 60min内产生氧气(mL) | 0.0 | 41.0 | 4.5 | 12.1 | 2.0 | 650.0 |
(1)实验②中应加入过氧化氢溶液的体积x是6mL.
(2)实验①~⑥通过测定相同时间内产生氧气的体积来比较过氧化氢的分解速率,还可以通过测定产生相同体积的氧气所需的时间来比较过氧化氢的分解速率.
(3)得出“过氧化氢溶液的浓度越大分解速率越大”结论所依据的实验是③④(填序号).
(4)通过实验①、②、④可得出的结论是温度越高,过氧化氢分解速率越大.
【反思与评价】
(5)同学们认为实验室制氧气,应选择实验⑥而不选实验②的理由是相同时间内实验②产生氧气少;需要加热;水蒸气含量高(答两点).
(6)某同学改用如图2所示装置代替气囊完成实验②,正确的实验操作顺序是a.
a.将导管伸入量筒,开启控温加热器,滴入过氧化氢溶液
b.开启控温加热器,将导管伸入量筒,滴入过氧化氢溶液
c.开启控温加热器,滴入过氧化氢溶液,待导管口有连续均匀气泡冒出时将导管伸入量筒.
 “可燃冰”(如图)主要成分是甲烷水合物,主要分布于深海沉淀物或陆域永久冻土中、1立方米的“可燃冰”可在常温下释放164立方米的甲烷和0.8立方米的淡水,被认为是一种潜力较大的能源之一.通常情况下,甲烷是没有颜色,没有气味的气体,比空气轻,极难溶于水.很容易燃烧
“可燃冰”(如图)主要成分是甲烷水合物,主要分布于深海沉淀物或陆域永久冻土中、1立方米的“可燃冰”可在常温下释放164立方米的甲烷和0.8立方米的淡水,被认为是一种潜力较大的能源之一.通常情况下,甲烷是没有颜色,没有气味的气体,比空气轻,极难溶于水.很容易燃烧