题目内容
14.实验室里用加热灼烧的方法来测定石灰石中碳酸钙(CaCO3)的质量分数.某化学兴趣小组将12g石灰石进行充分的灼烧后,得到白色固体7.6.(杂质不分解)(1)反应产生的二氧化碳的质量是4.4g
(2)计算石灰石中碳酸钙的质量分数.
分析 (1)根据碳酸钙受热分解生成氧化钙和二氧化碳,反应前后的质量差即为反应生成二氧化碳的质量;
(2)根据二氧化碳的质量可以计算碳酸钙的质量,进一步可以计算石灰石样品中碳酸钙的质量分数
解答 解:(1)生成二氧化碳质量为:12g-7.6g=4.4g;
(2)设12g石灰石中含CaCO3的质量为x
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 44
x 4.4g
$\frac{100}{x}$=$\frac{44}{4.4g}$
x═10g
所以CaCO3%═$\frac{10g}{12g}$×100%=83.3%
故答案为:(1)4.4g;
(2)83.3%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
2.1902年诞生于比利时的传统水处理工艺(经典“四部曲”)被美国工程院列为人类20世纪最重要的发明之一,其净水的方法主要有:①过滤,②絮凝,③消毒,④沉淀.下列最为合理的净水顺序是( )
| A. | ②①③④ | B. | ④②①③ | C. | ②④①③ | D. | ②④③① |
3.下列属于化学变化的是( )
| A. | 石蜡融化 | B. | 潮湿的衣服被晾干了 | ||
| C. | 铁生锈 | D. | 瓷碗破碎 |
2.2.4g铁和镁的混合物,与50.0g盐酸恰好完全反应,则该盐酸的溶质质量分数可能是( )
| A. | 5.0% | B. | 10.0% | C. | 15.0% | D. | 16.0% |
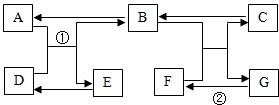 A~G是初中所学的常见物质,其转化关系如下图所示(部分反应物和生成物、反应条件已略去),A、B常温下为无色气体且组成元素相同,C是大理石的主要成分,D为红色固体,E为黑色固体.请回答下列问题:
A~G是初中所学的常见物质,其转化关系如下图所示(部分反应物和生成物、反应条件已略去),A、B常温下为无色气体且组成元素相同,C是大理石的主要成分,D为红色固体,E为黑色固体.请回答下列问题: