题目内容
10.配平下列方程式并计算各物质之间的质量比(1)C2H2+O2$\frac{\underline{\;点燃\;}}{\;}$CO2+H2O
(2)C+CO2$\frac{\underline{\;高温\;}}{\;}$CO.
分析 根据质量守恒定律:反应前后各原子的数目不变,选择相应的配平方法(最小公倍数法、定一法等)进行配平即可;配平时要注意化学计量数必须加在化学式的前面,配平过程中不能改变化学式中的下标;配平后化学计量数必须为整数.
利用各物质之间的质量比等于相对分子质量和的比,进行分析解答即可.
解答 解:(1)本题可利用“定一法”进行配平,把C2H2的化学计量数定为1,则O2、H2O、CO2前面的化学计量数分别为:$\frac{5}{2}$、1、2,同时扩大2倍,则C2H2、O2、CO2、H2O前面的化学计量数分别为2、5、4、2.
反应的化学方程式为:2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O;四种物质的质量比为(26×2):(32×5):(44×4):(18×2)=13:40:44:9.
(2)本题可利用“定一法”进行配平,把CO2的化学计量数定为1,则C、CO前面的化学计量数分别为:1、2.
反应的化学方程式为:C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO;三种物质的质量比为12:44:(28×2)=3:11:14.
故答案为:(1)2、5、4、2;13:40:44:9;(2)1、1、2;3:11:14.
点评 本题难度不大,掌握化学方程式的配平方法、化学反应中各物质之间的质量比等于相对分子质量和的比是正确解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.我们知道物质的性质决定事实上用途,下列物质的用途,体现其物理性质( )
| A. | 用氢气做高能燃料 | B. | 充入稀有气体使灯炮耐用 | ||
| C. | 用木炭来还原氧化铜 | D. | 用铁锅做饭 |
15.下列物质中属于酸式盐的是( )
| A. | K2CO3 | B. | NH4Cl | C. | NaHSO4 | D. | BaSO4 |
4.下列有关叙述中,正确的是( )
| A. | 可用肥皂水区别硬水和软水 | |
| B. | 要保护水资源,只能禁止使用化肥和农药 | |
| C. | 为了控制空气中PM2.5的含量应停止建筑工地施工 | |
| D. | 因为有了温室效应,全球平均地表温度才提高到适合人类生存的15℃ |
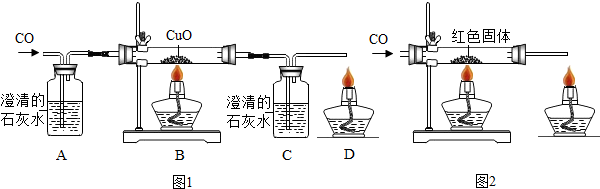
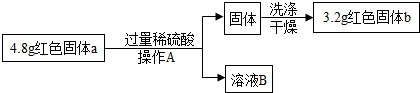
 能源是人类生存和发展的基础,能源成为人们日益关注的问题.
能源是人类生存和发展的基础,能源成为人们日益关注的问题.