题目内容
17.下列各组物质的溶液混和后,不一定会出现沉淀的是( )| A. | Na2SO4、BaCl2、HNO3 | B. | KNO3、Na2CO3、CaCl2 | ||
| C. | AgNO3、NaCl、HCl | D. | MgSO4、NaOH、H2SO4 |
分析 根据题意,各组物质的溶液混和后,不一定会出现沉淀,有酸存在的组合,要考虑组内物质混合生成的沉淀是否溶于酸,据此结合盐的化学性质,进行分析判断.
解答 解:A、Na2SO4、BaCl2混合产生不溶于硝酸的硫酸钡白色沉淀,一定会出现沉淀,故选项错误.
B、Na2CO3、CaCl2混合产生碳酸钙白色沉淀,一定会出现沉淀,故选项错误.
C、AgNO3与NaCl、HCl混合产生不溶于酸的氯化银白色沉淀,一定会出现沉淀,故选项错误.
D、硫酸镁与氢氧化钠混合能产生氢氧化镁白色沉淀,氢氧化镁能与硫酸反应生成硫酸镁和水,若硫酸过量,不会出现沉淀,故选项正确.
故选:D.
点评 本题难度不大,熟练掌握盐的化学性质、常见的难溶于酸的沉淀是正确解答本题的关键.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案
相关题目
7. 如图是甲、乙、丙三种固体物质的溶解度曲线,下列叙述正确的是( )
如图是甲、乙、丙三种固体物质的溶解度曲线,下列叙述正确的是( )
 如图是甲、乙、丙三种固体物质的溶解度曲线,下列叙述正确的是( )
如图是甲、乙、丙三种固体物质的溶解度曲线,下列叙述正确的是( )| A. | t2℃时,20g丙能溶解于50g水中形成70g溶液 | |
| B. | 若要将N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法 | |
| C. | t1℃时,等质量的甲、乙溶液中所含溶质的质量为乙>甲 | |
| D. | 分别将三种物质的饱和溶液从t3℃降温至t2℃时,所得溶液溶质质量分数的大小关系为乙>甲=丙 |
8.下列有关水的说法中正确的是( )
| A. | 应用水的硬度越小,越有利于人体健康 | |
| B. | 加入肥皂水振荡,产生的泡沫越多水的硬度越大 | |
| C. | 水分子中氢、氧元素的质量比是一定的 | |
| D. | 有水生成的反应一定没有化合价变化 |
5.下列实验操作正确的是( )
| A. | 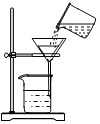 过滤 | B. | 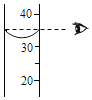 读取液体体积 | C. | 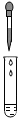 滴加液体 | D. | 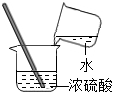 稀释浓硫酸 |
2.根据如图实验流程,下列分析正确的是( )
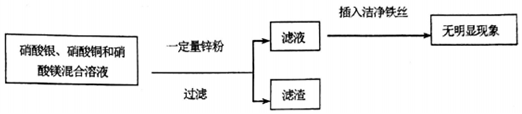

| A. | 滤液中一定有硝酸镁,可能有硝酸锌和硝酸亚铁 | |
| B. | 滤渣中一定有银和铜,可能有锌 | |
| C. | 滤渣中一定有银和铜,可能有镁 | |
| D. | 滤液中一定有硝酸镁和硝酸锌,可能有硝酸铜 |
9.下列有关物质组成的说法正确的是( )
| A. | 煤、石油、天然气都是化石能源,属于混合物 | |
| B. | 塑料、合成橡胶、合金都属于合成材料 | |
| C. | 氧气、白磷、硫都是具有可燃性的单质 | |
| D. | 煤气是由一氧化碳、甲烷、氢气等组成的有机物 |

 结合水和溶液的相关知识,回答下列问题:
结合水和溶液的相关知识,回答下列问题: