题目内容
16.根据装置图回答下列问题:(所用装置图用序号表示)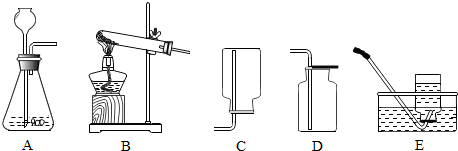
①检查装置A气密性的方法是用止水夹夹住导管上的胶皮管,再向长颈漏斗内注入水至浸没下端管口,再加水,长颈漏斗内液面不下降,说明不漏气;装置A中长颈漏斗的下端应伸入液面以下是为了防止气体从长颈漏斗溢出.
②实验室用高锰酸钾加热制取氧气应选用装置B和D或E连接;反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
③实验室制取二氧化碳时,应选用装置A和D 连接;反应的化学方程式:CaCO3+2HCl═CaCl2+CO2↑+H2O.
加热
④在实验室中,常用加热固体NH4Cl和Ca(OH)2混合物的方法制取氨气,其反应的化学方程式为:2NH4Cl+Ca(OH)2═CaCl2+2H2O+2NH3↑.已知在标准状况下,氨气的密度为0.77lg/L,空气的密度为l.293g/L,且在常温常压下,l体积水能溶解700体积的氨气.则实验室制取氨气应选用装置B和C 连接.
分析 ①据A装置检验气密性的方法及实验注意事项解答;
②依据反应物状态、反应条件选择发生装置,根据气体的密度和溶解性选择收集装置;
③实验室制CO2用固体碳酸钙和液体盐酸反应,因为反应不需要加热,根据二氧化碳的物理性质来分析收集方法;
④根据发生和收集装置的选取方法分析回答.
解答 解:①用止水夹夹住导管上的胶皮管,再向长颈漏斗内注入水至浸没下端管口,再加水,长颈漏斗内液面不下降,说明不漏气;装置A中长颈漏斗的下端应伸入液面以下是为了防止气体从长颈漏斗溢出
②实验室用高锰酸钾加热制取氧气为固体加热反应,发生装置选择B;生成的氧气密度比空气大,不易溶于水故可选用D或E收集氧气;反应的方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
③实验室用大理石和稀盐酸反应制取二氧化碳,属于固体和液体混合不需加热,故选A发生装置,二氧化碳的密度比空气大且能溶于水,故只能用向上排空气收集;碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑;
④用加热氯化铵固体和氢氧化钙固体混合物的方法制取氨气,属于固体加热型,故选发生装置B;氨气密度小于空气密度,极易溶于水,故只能用向下排空气法收集;
故答案为:①用止水夹夹住导管上的胶皮管,再向长颈漏斗内注入水至浸没下端管口,再加水,长颈漏斗内液面不下降,说明不漏气、防止气体从长颈漏斗溢出;
②B、D或E、2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
③A、D、CaCO3+2HCl=CaCl2+H2O+CO2↑;
④B、C.
点评 本题主要考查了氧气、二氧化碳的反应装置、收集方法及反应原理.

| A. | 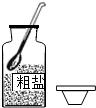 取用固体 | B. | 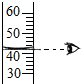 读取液体体积 | C. | 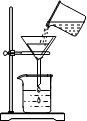 过滤 | D. |  滴加液体 |
| A. | 2NO:两个一氧化氮分子 | B. | Mg2+:镁元素的化合价是+2 | ||
| C. | 2O:两个氧分子 | D. | H2O:一个水分子中有两个氢分子 |
| A. | Ag | B. | Mg | C. | Cu | D. | Zn |
| A. | 反应类型为化合反应 | B. | 该反应中氧气表现出氧化性 | ||
| C. | 反应前后Co3O4质量改变 | D. | 反应前后碳元素的化合价改变 |
| A. | 液氧 | B. | 清澈的泉水 | C. | 冰水 | D. | 干冰 |
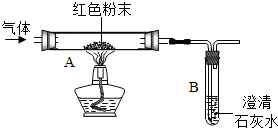 类比法是化学研究物质的重要方法之一.草酸的化学性质与碳酸相似.已知碳酸易分解,草酸在受热条件下也分解,仅生成三种氧化物.某校研究性学习小组对此展开探究:
类比法是化学研究物质的重要方法之一.草酸的化学性质与碳酸相似.已知碳酸易分解,草酸在受热条件下也分解,仅生成三种氧化物.某校研究性学习小组对此展开探究: