题目内容
建国60多年来,我国化学基础科学的发展,取得了举世瞩目的成就.我国科学家用滤纸和二氧化钛(TiO2)薄膜制作出一种新型“纳米纸”,又在纳米纸上“铺”一层“萘胺”(C10H9N)染料,制成一种试纸,用于检测食品中亚硝酸盐浓度的高低.
(1)二氧化钛中Ti的化合价为 .
(2)萘胺的一个分子中,C、H、N三种原子的个数之比为 (填最简整数比).
(3)已知NaNO2能发生如下反应(化学方程式已配平):
2NaNO2+2KI+2H2SO4=I2+2M↑+2H2O+Na2SO4+K2SO4,则M的化学式是 .
(4)根据上述反应,可用化学试纸及生活中常见物质进行实验来鉴别亚硝酸盐和食盐,现有碘化钾淀粉试纸,则还需选用下列生活中的常见物质为 (填序号).
①食用油 ②白酒 ③食醋 ④牛奶.
(1)二氧化钛中Ti的化合价为
(2)萘胺的一个分子中,C、H、N三种原子的个数之比为
(3)已知NaNO2能发生如下反应(化学方程式已配平):
2NaNO2+2KI+2H2SO4=I2+2M↑+2H2O+Na2SO4+K2SO4,则M的化学式是
(4)根据上述反应,可用化学试纸及生活中常见物质进行实验来鉴别亚硝酸盐和食盐,现有碘化钾淀粉试纸,则还需选用下列生活中的常见物质为
①食用油 ②白酒 ③食醋 ④牛奶.
考点:有关元素化合价的计算,质量守恒定律及其应用,鉴别淀粉、葡萄糖的方法与蛋白质的性质
专题:结合课本知识的信息
分析:(1)根据在化合物中正负化合价代数和为零,结合二氧化钛的化学式进行解答本题.
(2)根据萘胺的一个分子的构成进行分析解答.
(3)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物M的化学式.
(4)鉴别NaNO2和NaCl,可根据NaNO2在酸性条件下与碘化钾反应生成碘,进行分析解答.
(2)根据萘胺的一个分子的构成进行分析解答.
(3)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物M的化学式.
(4)鉴别NaNO2和NaCl,可根据NaNO2在酸性条件下与碘化钾反应生成碘,进行分析解答.
解答:解:(1)氧元素显-2价,设钛元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×2=0,则x=+4价.
(2)1个萘胺分子是由10个碳原子、9个氢原子和1个氮原子构成的,则萘胺分子中C、H、N的原子个数比为10:9:1.
(3)根据反应的化学方程式2NaNO2+2KI+2H2SO4=I2+2M↑+2H2O+Na2SO4+K2SO4,反应物中钠、氮、氧、钾、碘、氢、硫原子个数分别为2、2、12、2、2、4、2,反应后的生成物中钠、氮、氧、钾、碘、氢、硫原子个数分别为2、0、10、2、2、4、2,根据反应前后原子种类、数目不变,则2M中含有2个氮原子和2个氧原子,则每个M分子由1个氮原子和1个氧原子构成,则物质M的化学式为NO.
(4)鉴别NaNO2和NaCl,可根据NaNO2在酸性条件下与碘化钾反应生成碘,故可用淀粉碘化钾试纸来检验,可加入醋酸酸化.
故答案为:(1)+4;(2)10:9:1;(3)NO;(4)③.
(2)1个萘胺分子是由10个碳原子、9个氢原子和1个氮原子构成的,则萘胺分子中C、H、N的原子个数比为10:9:1.
(3)根据反应的化学方程式2NaNO2+2KI+2H2SO4=I2+2M↑+2H2O+Na2SO4+K2SO4,反应物中钠、氮、氧、钾、碘、氢、硫原子个数分别为2、2、12、2、2、4、2,反应后的生成物中钠、氮、氧、钾、碘、氢、硫原子个数分别为2、0、10、2、2、4、2,根据反应前后原子种类、数目不变,则2M中含有2个氮原子和2个氧原子,则每个M分子由1个氮原子和1个氧原子构成,则物质M的化学式为NO.
(4)鉴别NaNO2和NaCl,可根据NaNO2在酸性条件下与碘化钾反应生成碘,故可用淀粉碘化钾试纸来检验,可加入醋酸酸化.
故答案为:(1)+4;(2)10:9:1;(3)NO;(4)③.
点评:本题难度不大,掌握利用化合价的原则计算指定元素的化合价的方法、化学式的含义、化学反应前后原子守恒来确定物质的化学式的方法等即可正确解答本题.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
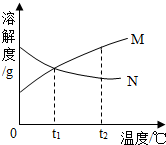 如图是M、N两种物质的溶解度曲线,由溶解度曲线得出以下几条信息,你认为正确的是( )
如图是M、N两种物质的溶解度曲线,由溶解度曲线得出以下几条信息,你认为正确的是( )| A、t1℃时,M、N两物质溶液溶质质量分数相等 |
| B、由t1℃升温到t2℃时,N物质溶液溶质质量分数不变 |
| C、M物质的溶解度大于N物质的溶解度 |
| D、N物质的溶解度随温度的升高而降低 |
低碳,生活中就是要节能、减少一次性物品消耗.下列不属于“低碳”行为的是( )
| A、少用冰箱储存食物 |
| B、出门时随手关闭电器电源 |
| C、购物时尽量使用一次性塑料袋 |
| D、用节能灯替换家里的白炽灯泡 |
下列变化属于化学变化的是( )
| A、钢铁生锈 | B、干冰升华 |
| C、滴水成冰 | D、拨云见日 |
下列物品中,不属于有机高分子合成材料制品的是( )
| A、矿泉水瓶 | B、游戏手柄 |
| C、篮球 | D、水泥 |