题目内容
6.某石灰水中含有氢氧化钙2.96g,如果该石灰水吸收二氧化碳完全反应变成白色沉淀,则可以吸收二氧化碳的质量是多少?分析 氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,根据氢氧化钙的质量可以计算需要二氧化碳的质量.
解答 解:设吸收二氧化碳的质量为x
Ca(OH)2+CO2=CaCO3↓+H2O
74 44
2.96g x
$\frac{74}{44}=\frac{2.96g}{x}$
解得x=1.76g
答:吸收二氧化碳的质量为1.76g.
点评 本题主要考查学生运用化学方程式进行计算和推断的能力,比较简单,计算时要注意规范性和准确性即可.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
10.分类、类比是学习化学变化常用的方法.
(1)初中化学有许多实验,若按照实验主要目的可将实验分为:探究化学反应前后物质的质量关系、探究物质的性质、探究物质的含量等.据此应将下列实验中的D与A(填“A”或“B”或“C”)归为一类,依据是D实验和A实验的主要目的都是探究物质的性质.
(2)许多物质的命名与元素的化合价高地有关,如锰酸钾、高锰酸钾,其中锰元素的化合价分别为+6、+7.氯元素常见的化合价有+7、+5、+1、-1等,由此推测钠元素、氧元素和+7价氯元素三种元素组成的化合物的名称为高氯酸钠,化学式为NaClO4.
(1)初中化学有许多实验,若按照实验主要目的可将实验分为:探究化学反应前后物质的质量关系、探究物质的性质、探究物质的含量等.据此应将下列实验中的D与A(填“A”或“B”或“C”)归为一类,依据是D实验和A实验的主要目的都是探究物质的性质.
 |  |
| A | B |
 |  |
| C | D |
17.某同学对酸碱盐的知识进行了以下的梳理.
(1)现有如下表格物质:它们都属于盐(填 酸、碱、盐)
反思:根据以上物质中的金属元素的排列,可以得出是依据金属活动性顺序 顺序归纳整理的.
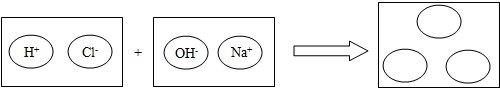
(2)为理解稀盐酸和氢氧化钠两者之间发生反应的微观实质,绘制了如图.请你在右边的圆圈中填入适当的化学式或离子符号:
(1)现有如下表格物质:它们都属于盐(填 酸、碱、盐)
| 氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | 氯化亚铁 | 氯化铜 |
| KCl | CaCl2 | NaCl | MgCl2 | AlCl3 | ZnCl2 | FeCl2 | CuCl2 |
(2)为理解稀盐酸和氢氧化钠两者之间发生反应的微观实质,绘制了如图.请你在右边的圆圈中填入适当的化学式或离子符号:

1.某病人静脉注射了质量分数为5%的葡萄糖注射液500g,其中含葡萄糖(C6H12O6)的质量是( )

| A. | 125 g | B. | 100 g | C. | 50 g | D. | 25 g |
11.以下是生活常见现象或结论,正确的是( )
| A. | 为了加强农作物产量,要尽可能多的使用农药 | |
| B. | 工业排污水会造成水体污染 | |
| C. | 在室内放盆水能防止CO中毒 | |
| D. | 塑料是有机合成材料,不能把它投进带有 标志的垃圾桶 标志的垃圾桶 |
15.下列各选项中不属于化学反应的是( )
| A. | 用活性炭除去冰箱中的异味 | B. | 用胃舒平治疗胃酸过多 | ||
| C. | 在蔗糖中加入浓硫酸后变黑 | D. | 煤的干馏 |
16.下列有关化学科学认识正确的是( )
| A. | 一定条件下可用石墨制得金刚石 | B. | “绿色食品”就是绿颜色的食品 | ||
| C. | 氮气不与任何物质反应 | D. | 纯牛奶中不含任何化学物质 |
