题目内容
17.某同学对酸碱盐的知识进行了以下的梳理.(1)现有如下表格物质:它们都属于盐(填 酸、碱、盐)
| 氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | 氯化亚铁 | 氯化铜 |
| KCl | CaCl2 | NaCl | MgCl2 | AlCl3 | ZnCl2 | FeCl2 | CuCl2 |
(2)为理解稀盐酸和氢氧化钠两者之间发生反应的微观实质,绘制了如图.请你在右边的圆圈中填入适当的化学式或离子符号:
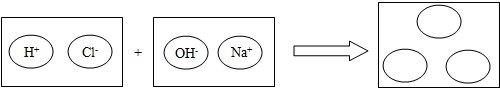
分析 根据已有的物质的类别进行分析解答,盐是由金属离子和酸根离子组成的化合物,根据盐中金属的活动性分析解答,酸碱反应的实质是酸中的氢离子和碱中的氢氧根离子结合生成水分子的过程.
解答 解:(1)根据表格提供的物质的化学式的组成可以看出,这些物质都是由金属离子和氯离子组成的化合物,属于盐,在金属活动性顺序中,这些盐中所含的金属的活动性依次减弱,故填:盐,金属活动性;
(2)酸碱反应的实质是酸中的氢离子和碱中的氢氧根离子结合生成水分子,而金属钠离子和酸根离子氯离子仍然是以自由移动的离子存在,故填:H2O,Na+,Cl-.
点评 本题考查的是常见的物质的类别和酸碱反应的实质的知识,掌握有关物质的概念以及酸碱反应的实质是正确解答本题的关键.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
1.水是宝贵的自然资源,下列净化水的方法中,净化程度最高的是( )
| A. | 蒸馏 | B. | 沉淀 | C. | 过滤 | D. | 吸附 |
2. 如图是反映某个化学反应里个物质质量与时间的变化关系,下列对此变化的描述中,正确的是( )
如图是反映某个化学反应里个物质质量与时间的变化关系,下列对此变化的描述中,正确的是( )
 如图是反映某个化学反应里个物质质量与时间的变化关系,下列对此变化的描述中,正确的是( )
如图是反映某个化学反应里个物质质量与时间的变化关系,下列对此变化的描述中,正确的是( )| A. | 充分反应后,乙+丙=甲的质量 | |
| B. | 物质甲的相对分子质量大于乙 | |
| C. | 此化学反应中,不遵守质量守恒定律 | |
| D. | 此化学反应是分解反应 |
9.下列相关事实用微粒的观点解释正确的是( )
| 选项 | 事 实 | 解 释 |
| A | 食盐在冷水中溶解得更慢 | 氯化钠分子运动速率随温度降低而减慢 |
| B | 夏天氦气球在阳光下曝晒过久易爆炸 | 氦原子间的间隔随温度的升高而增大 |
| C | 一氧化碳有可燃性而二氧化碳不可燃 | 构成分子的原子的种类不同 |
| D | 氢氧化钾溶液能使紫色石蕊溶液变蓝 | 在水中会解离出钾离子和氢氧根离子 |
| A. | A | B. | B | C. | C | D. | D |