题目内容
6.金属铝是世界上仅次于钢铁的第二重要金属,由于铝具有密度小、导电导热性好,易于机械加工及其他许多优良性能,因而广泛应用于国民经济各部门.福建省有丰富的铝土矿,拟用铝土矿(主要成分Al2O3,还有少量Fe2O3,SiO2)为原料冶炼铝,工艺流程如图所示: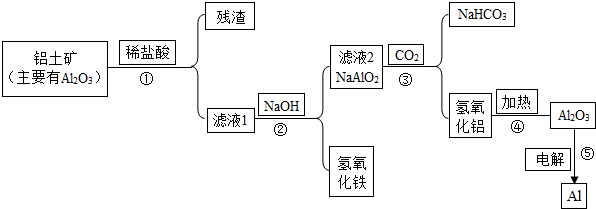
(1)通过上述材料得知,铝具有的物理性质有密度小、导电导热性好,易于机械加工.
(2)早在春秋战国时期,我国就开始生产和使用铁器,但铝的利用要比铁晚得多,其主要原因是铝比铁活泼.
(3)已知上述反应②中生成氢氧化铁沉淀是发生了复分解反应,请写出该反应的化学方程式FeCl3+3NaOH=Fe(OH)3↓+3NaCl.
(4)已知上述反应⑤为分解反应,另一产物是气体单质,该反应的化学方程式为2Al2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑.
(5)铝土矿中的Fe2O3在工业上常利用一氧化碳来还原冶炼出金属铁,该反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(6)金属资源十分有限,而且不能再生,保护金属资源的一种有效途径是防止金属的腐蚀,要防止铁生锈的措
施有喷漆.
分析 (1)不需要发生化学变化就表现出来的性质属于物质的物理性质;
(2)根据金属的活动性顺序来分析;
(3)氯化铁与氢氧化钠反应生成氢氧化铁沉淀和氯化钠;
(4)氧化铝在通电的条件反应生成铝和氧气;
(5)一氧化碳与氧化铁在高温下反应生成铁与二氧化碳;
(6)某些金属暴露在空气中时容易生锈,防止金属生锈的方法通常是把金属和空气或水隔绝.
解答 解:(1)密度小、导电导热性好,易于机械加工属于铝的物理性质;故填:密度小、导电导热性好,易于机械加工;
(2)因为铝的活动性比铁强,所以铝的利用要比铁晚得多,故填:铝比铁活泼;
(3)氯化铁与氢氧化钠反应生成氢氧化铁沉淀和氯化钠,该反应属于基本反应类型中的复分解反应,故填:FeCl3+3NaOH=Fe(OH)3↓+3NaCl;
(4)氧化铝在通电的条件下,分解为铝和氧气;故填:2Al2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑;
(5)一氧化碳与氧化铁在高温下发生反应生成铁与二氧化碳,故答案为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(6)常见的金属采用的防锈措施是喷漆或刷油漆或涂油.
故填:喷漆(其他合理答案也可).
点评 本题考查了金属的性质、方程式的书写、金属的防锈措施,解答本题的关键是掌握防止金属生锈的方法方面的知识,只有这样才能对问题做出正确的判断.

练习册系列答案
相关题目
17.“信息”“材料”和“能源”被称为新科技革命的三大支柱.下列叙述不正确的是( )
| A. | 化石能源、核能均属于不可再生能源 | |
| B. | 宇宙飞船的制造,使用了大量新型材料 | |
| C. | 有机高分子材料的广泛应用“有百利而无一害” | |
| D. | 人类应与环境和谐相处,要合理开发和利用矿物资源 |
14. 我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研究中获得重大突破.其成果在最近的美国《科学》杂志发表.该转化的微观示意图如图所示.有关说法错误的是( )
我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研究中获得重大突破.其成果在最近的美国《科学》杂志发表.该转化的微观示意图如图所示.有关说法错误的是( )
 我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研究中获得重大突破.其成果在最近的美国《科学》杂志发表.该转化的微观示意图如图所示.有关说法错误的是( )
我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研究中获得重大突破.其成果在最近的美国《科学》杂志发表.该转化的微观示意图如图所示.有关说法错误的是( )| A. | 该反应属于分解反应 | B. | 催化剂改变了反应速率 | ||
| C. | 生成物之一为C2H4 | D. | 反应物与生成物共有4种分子 |
11.下列变化中,能证明分子可分的事实是( )
| A. | 硬水通过蒸馏可以软化 | |
| B. | 用过滤的方法除去海水中的难溶性物质 | |
| C. | 水在直流电的作用下变成氢气和氧气 | |
| D. | 浑浊的水加明矾得到净化 |
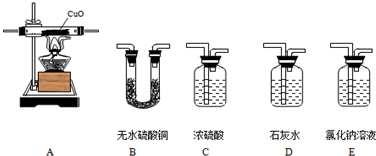
 如图为一氧化碳还原氧化铜的装置图:
如图为一氧化碳还原氧化铜的装置图:
