题目内容
5.为了证明铁、银、铜三种金属的活动性顺序,同学们设计了如下实验:(1)方案一:将厚薄和形状相同的铁片、银片、铜片分别放入同体积10%的稀硫酸中,观察到的现象是铁片的表面有气泡产生,溶液由无色变为浅绿色;银片、铜片的表面无气泡产生发生反应的化学方程式为Fe+H2SO4═FeSO4+H2↑.由此证明铁比银和铜活泼,为了证明银和铜的金属活动性顺序,可将银片放入硫酸铜溶液中,看到银片表面无明显现象;还可以将铜片放入硝酸银溶液中,观察到的现象是铜片表面析出黑色(银白色)固体,(溶液由无色变成蓝色)
(2)方案二:只需将铁片、银片、铜片中的两种金属分别放入一种溶液中,即可验证三种金属的活动性强弱,所用的溶液是硫酸铜溶液
(3)方案三:…
分析 根据金属活动性顺序及其应用回答,活泼金属能置换出酸中的氢,排在前面的金属能把排在它后面的金属从盐溶液中置换出来.化学反应中伴随的现象主要是由生成物的性质决定的,书写化学方程式时要注意配平和条件;比较三种金属的活动性顺序,要依次证明每两种金属的活动性强弱.
解答 解:(1)将铁片浸入稀硫酸中能产生氢气,说明铁排在氢的前面,将银片、铜片浸入稀硫酸中,不反应说明银排在氢的后面;铁片的表面有气泡产生,溶液由无色变为浅绿色;银片、铜片的表面无气泡产生;反应的化学方程式为Fe+H2SO4═FeSO4+H2↑;铜的活动性比银强,因此铜会把硝酸银中的银置换出来,观察到的现象为:铜片表面析出黑色(银白色)固体,(溶液由无色变成蓝色);
(2)金属与盐反应说明金属排在盐中金属的前面,金属与盐不反应,说明金属排在了盐中金属的后面,所以加入的盐溶液应该位于两种金属之间;由于三种金属的活动性铜在中间,所以两种金属放到硫酸铜溶液中即可;
故答案为:(1)铁片的表面有气泡产生,溶液由无色变为浅绿色;银片、铜片的表面无气泡产生;Fe+H2SO4═FeSO4+H2↑;铜片表面析出黑色(银白色)固体,(溶液由无色变成蓝色);
(2)硫酸铜溶液.
点评 本题难度不大,考查金属活动性应用,氢前金属可与盐酸、硫酸反应,氢后金属则不能;前面的金属可将后面的金属从其盐溶液中置换出来,据此可设计实验验证金属的活动性顺序.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
13.世界上最轻材料“碳海绵”的主要成分是石墨烯和碳纳米管(两者都是碳单质),具备高弹性和疏松多孔的结构,它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状.下列关于“碳海绵”的说法中,不正确的是( )
| A. | 碳海绵可燃烧 | B. | 碳海绵可处理海上石油泄漏 | ||
| C. | 碳海绵可重复使用 | D. | 常温下碳海绵化学性质活泼 |
10.地壳中含量最多的非金属元素X与含量最多的金属元素Y形成的化合物的化学式是( )
| A. | X2Y3 | B. | Y2X3 | C. | X2Y | D. | YX2 |
17.“环境保护,人人有责”.影响空气质量的是一组主要污染物是( )
| A. | SO2 NO2 可吸入颗粒物 | B. | CO2 NO2 O2 | ||
| C. | CO2 SO2 N2 | D. | SO2 CO2 可吸入颗粒物 |
14.下列物质分别和98克10%的硫酸溶液恰好完全反应,其中所得溶液中溶质质量分数最小的是( )
| A. | Zn | B. | ZnO | C. | Zn(OH)2 | D. | ZnCO3 |
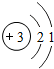 金属-锂(Li),被称为“21世纪的能源金属”,当前手机中广泛使用的电池,主要是高能锂电池.请回答下列问题:
金属-锂(Li),被称为“21世纪的能源金属”,当前手机中广泛使用的电池,主要是高能锂电池.请回答下列问题: