题目内容
13.向NaOH溶液中不断滴加稀盐酸,溶液pH随加入盐酸体积变化与如图相符的是( )| A. |  盐酸的体积 | B. |  盐酸的体积 | C. |  盐酸的体积 | D. |  盐酸的体积 |
分析 根据氢氧化钠溶液显碱性,碱性溶液的pH大于7;向NaOH溶液中不断滴加盐酸溶液时,盐酸与氢氧化钠发生中和反应生成氯化钠和水,氯化钠溶液呈中性,中性溶液的pH等于7;由于氢氧化钠减少,所以溶液的pH不断减小,当盐酸与氢氧化钠恰好完全发生时,溶液呈中性,溶液的pH等于7;再滴加稀盐酸,溶液显酸性,溶液的pH小于7进行分析.
解答 解:A、氢氧化钠和盐酸反应生成氯化钠和水,所以pH值会逐渐减小,故A错误;
B、因为当最终加入的盐酸过量时,溶液显酸性,所以终点应在7的下方,故B错误;
C氢氧化钠溶液显碱性,碱性溶液的pH大于7;向NaOH溶液中不断滴加盐酸溶液时,盐酸与氢氧化钠发生中和反应生成氯化钠和水,氯化钠溶液呈中性,中性溶液的pH等于7,由于氢氧化钠减少,所以溶液的pH不断减小,当盐酸与氢氧化钠恰好完全发生时,溶液呈中性,溶液的pH等于7,再滴加稀盐酸,溶液显酸性,溶液的pH小于7,故C正确;
D、氢氧化钠的pH值大于7,所以刚开始,溶液的pH值不会从零开始,故D错误.
故选:C.
点评 这是一道函数图象的考题,重点考查了酸和碱的pH以及酸碱中和的问题,是考试的重点.

练习册系列答案
相关题目
8.发明了“联合制碱法”的科学家是( )
| A. |  侯德榜 | B. |  拉瓦锡 | C. |  门捷列夫 | D. |  张青莲 |
9.有NaHCO3和Na2CO3混合物13.7g,将其充分加热至固体质量不再减少,得剩余固体.将产生的气体通入足量的Ca(OH)2溶液中,产生5.0g沉淀.下列说法正确的是( )
| A. | 剩余固体为混合物 | |
| B. | 剩余固体的质量为11.5g | |
| C. | 原混合物中Na2CO3的质量大于NaHCO3 | |
| D. | 将剩余固体溶于足量的稀盐酸,产生4.4g CO2 |
1.科学的方法是实验成功的前提条件,老师常提出一些实验的方法或要求,下列各组方法或要求存在错误的是( )
| 组号 | 实验方法或要求 |
| A | ①做铁丝燃烧实验,氧气最好用排水法收集 ②做蜡烛燃烧实验,氧气要用向上排空气法收集 |
| B | ①做木炭在氧气中燃烧实验,木炭点燃后,要从集气瓶口缓缓伸到集气瓶底部 ②做测定空气中氧气含量实验,点燃红磷后,要立即塞紧橡皮塞 |
| C | ①用胶头滴管吸取液体时,要先挤瘪橡胶头,再将胶头滴管伸入到液体 ②制气体时,要先检查装置的气密性,再向装置中装入药品 |
| D | ①用洗洁精代替汽油来溶解玻璃仪器上的油污 ②用氢氧化钠固体代替氢氧化钠溶液和稀盐酸反应证明中和反应散热 |
| A. | A | B. | B | C. | C | D. | D |
18.可用酒精灯火焰直接加热的玻璃仪器是( )
| A. | 集气瓶 | B. | 烧杯 | C. | 量筒 | D. | 蒸发皿 |
5.下列从微观角度分析解释错误的是( )
| A. | 酒香不怕巷子深--分子总在不断的运动着 | |
| B. | 50ml酒精和50ml水相混合总体积小于100ml--分子之间有间隔 | |
| C. | 液态水变成水蒸气,体积增大--水分子的体积变大 | |
| D. | 氢气和液氢都可以做燃料--同种分子化学性质相同 |
2.在2N、N2、2CO、SO2中,数字“2”能用来表示分子个数的有( )
| A. | 1个 | B. | 2个 | C. | 4个 | D. | 5个 |
3.小聪同学家新换了水龙头,从说明书上了解到水龙头是铜质镀铬.好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱.
【查阅资料】
(1)铬是银白色有金属光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
【结论与解释】
(1)小聪得出Fe、Cu、Cr三种金属的活动性由强到弱的顺序是Cr>Fe>Cu.
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应.
【知识运用】
将铬片投入FeSO4溶液中,反应能(选填“能”或“不能”)进行.若能进行,请你写出反应的化学方程式Cr+FeSO4=Fe+CrSO4.
(3)配制农药波尔多液不能用铁制容器,用化学方程式解释Fe+CuSO4═FeSO4+Cu.
【查阅资料】
(1)铬是银白色有金属光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验操作 | 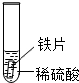 | 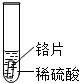 | 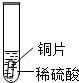 |
| 实验现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变为蓝色 | 无明显现象发生(或无气泡生成,溶液也不变色) |
(1)小聪得出Fe、Cu、Cr三种金属的活动性由强到弱的顺序是Cr>Fe>Cu.
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应.
【知识运用】
将铬片投入FeSO4溶液中,反应能(选填“能”或“不能”)进行.若能进行,请你写出反应的化学方程式Cr+FeSO4=Fe+CrSO4.
(3)配制农药波尔多液不能用铁制容器,用化学方程式解释Fe+CuSO4═FeSO4+Cu.